
 “盐水动力”玩具车的电池以镁片、活性炭为电极,向极板上滴加食盐水后电池便可工作,电池反应为2Mg+O2+2H2O=2Mg (OH)2下列关于该电池的说法错误的是( )
“盐水动力”玩具车的电池以镁片、活性炭为电极,向极板上滴加食盐水后电池便可工作,电池反应为2Mg+O2+2H2O=2Mg (OH)2下列关于该电池的说法错误的是( )| A. | Mg电极的电极反应式:Mg-2e-=Mg2+ | |
| B. | 这种电池的工作原理可以认为是镁的吸氧腐蚀 | |
| C. | 活性炭电极上发生氧化反应 | |
| D. | 电池工作时实现了化学能向电能的转化 |
分析 该装置是将化学能转化为电能的装置,Mg易失电子作负极、C作正极,正极上氧气得电子生成氢氧根离子,食盐水为电解质溶液,据此分析解答.
解答 解:A.Mg易失电子作负极,负极反应为Mg-2e-+2OH-=Mg(OH)2,故A错误;
B.负极Mg失电子,正极上氧气得电子,则电池的工作原理可以认为是镁的吸氧腐蚀,故B正确;
C.活性炭电极上氧气得电子发生还原反应,故C错误;
D.该电池为燃料电池,是将化学能转化为电能的装置,故D正确;
故选AC.
点评 本题考查化学电源新型电池,侧重考查基本概念、电池反应式的书写,注意电子流向、电解质溶液中离子流向,为易错点,侧重于考查学生的分析能力和应用能力.


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:选择题
| A. | c(OH-)=1×10-7mol/L | B. | c(H+)=1×10-7mol/L | ||
| C. | c(OH-)=c(H+) | D. | pH=7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.0 mol•L-1 | B. | 1.5 mol•L-1 | C. | 1 mol•L-1 | D. | 0.5 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 号序 | 物质 | 杂质 | 除杂质应选用的试剂或操作方法 |
| ① | KNO3 | KOH | 加入FeCl3溶液,并过滤 |
| ② | FeSO4 | CuSO4 | 加入足量铁粉后过滤 |
| ③ | O2 | CO2 | 依次通过盛有浓硫酸和NaOH溶液的洗气瓶 |
| ④ | CaO | CaCO3 | 加入稀盐酸,再蒸发 |
| A. | ①④ | B. | ② | C. | ②④ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
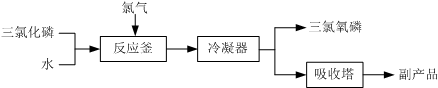
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 弱碱性溶液中可能大量存在Na+、K+、Cl-、HCO3- | |
| B. | 滴加石蕊呈红色的溶液可能大量存在K+、NH4+、Cl-、S2- | |
| C. | 与Al反应能放出H2的溶液中可能大量存在:Fe2+、K+、NO3-、SO42- | |
| D. | 漂白粉的水溶液可能大量存在Fe2+、Cl-、Ca2+、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4Cl溶液、NaOH溶液、碱石灰 | B. | 浓氨水、NaOH固体、浓硫酸 | ||
| C. | NH4Cl固体、消石灰、碱石灰 | D. | 浓NaOH溶液、NH4C固体、浓硫酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com