

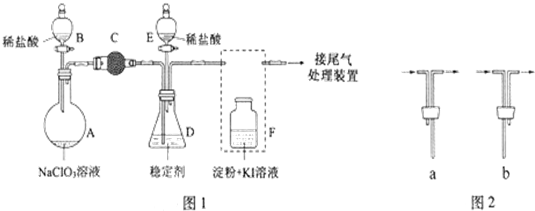
分析 装置B中制备得到ClO2,所以B中为NaClO3和Na2SO3在浓H2SO4的作用下生成ClO2和Na2SO4,反应方程式为2NaClO3+Na2SO3+H2SO4=2ClO2↑+2Na2SO4+H2O;
C可防止倒吸,起到安全瓶的作用;D中加入过氧化氢和氢氧化钠,在低温下与ClO2反应生成NaClO2,反应方程式为2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2;
A和E都为尾气处理装置,防止污染大气;
(1)装置D中发生气体反应,装置内压强降低,装置C的作用是安全瓶,防止D瓶溶液倒吸到B瓶中;
(2)装置B中制备得到ClO2,所以B中反应为NaClO3和Na2SO3在浓H2SO4的作用生成 ClO2和Na2SO4,装置D反应后的溶液获得NaClO2晶体,装置D中生成NaClO2,Cl元素的化合价降低,双氧水应表现还原性,有氧气生成,结合原子守恒可知,还有水生成,配平书写方程式;B制得的气体中含有SO2,在装置D中被氧化生成硫酸,可以用利用硫酸钡是白色沉淀检验硫酸根;
(3)由题目信息可知,应控制温度38℃~60℃,高于60℃时NaClO2分解成NaClO3和NaCl;
(4)②碘遇淀粉变蓝色,反应结束时,碘反应完全,滴加最后一滴Na2S2O3标准液时溶液蓝色恰好褪去且半分钟内不复原,说明到达滴定终点;
根据化学反应可得关系式:NaClO2~2I2~4S2O32-,令样品中NaClO2的物质的量x,根据方程式计算x值,根据m=nM计算次氯酸钠质量,其质量分数=$\frac{次氯酸钠质量}{样品质量}$.
解答 解:装置B中制备得到ClO2,所以B中为NaClO3和Na2SO3在浓H2SO4的作用下生成ClO2和Na2SO4,反应方程式为2NaClO3+Na2SO3+H2SO4=2ClO2↑+2Na2SO4+H2O;
C可防止倒吸,起到安全瓶的作用;D中加入过氧化氢和氢氧化钠,在低温下与ClO2反应生成NaClO2,反应方程式为2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2;
A和E都为尾气处理装置,防止污染大气;
(1)装置D中发生气体反应,装置内压强降低,装置C的作用是安全瓶,防止D瓶溶液倒吸到B瓶中,
故答案为:防止D瓶溶液倒吸到B瓶中;
(2)装置B中制备得到ClO2,所以B中反应为NaClO3和Na2SO3在浓H2SO4的作用生成 ClO2和Na2SO4,反应的方程式为2NaClO3+Na2SO3+H2SO4=2 ClO2↑+2Na2SO4+H2O,装置D反应后的溶液获得NaClO2晶体,装置D中生成NaClO2,Cl元素的化合价降低,双氧水应表现还原性,有氧气生成,结合原子守恒可知,还有水生成,配平后方程式为:2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2,B制得的气体中含有SO2,在装置D中被氧化生成硫酸,溶液中可能存在SO42-,用氯化钡溶液检验SO42-,具体操作:取少量反应后的溶液,先加足量的盐酸,再加BaCl2溶液,若产生白色沉淀,则说明含有SO42-,
故答案为:2NaClO3+Na2SO3+H2SO4=2ClO2↑+2Na2SO4+H2O;2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2;SO42-;取少量反应后的溶液,先加足量的盐酸,再加BaCl2溶液,若产生白色沉淀,则说明含有SO42-;
(3)由题目信息可知,应控制温度38℃~60℃,高于60℃时NaClO2分解成NaClO3和NaCl,所以如果撤去D中的冷水浴,可能导致产品中混有的杂质是NaClO3和NaCl,
故答案为:NaClO3和NaCl;
(4)碘遇淀粉变蓝色,反应结束时,碘反应完全,滴加最后一滴Na2S2O3标准液时溶液蓝色恰好褪去且半分钟内不复原,说明到达滴定终点,
②令样品中NaClO2的物质的量xmol,将所得混合液配成250mL待测溶液,移取25.00mL待测溶液于锥形瓶中则25.00mL次氯酸钠溶液中次氯酸钠的物质的量为0.1xmol,
NaClO2~2I2~4S2O32-,
1mol 4mol
0.1xmol c mol•L-1×V×10-3L
故1mol:4mol=0.1xmol:( c mol•L-1×V×10-3L)
x=$\frac{cmol/L×V×1{0}^{-3}L×1mol}{4mol×0.1mol}$=2.5×10-3c•V,
次氯酸钠质量分数=$\frac{2.5×1{0}^{-3}cVmol×90.5g/mol}{mg}$=$\frac{226.25cV}{m}$,
故答案为:滴加最后一滴Na2S2O3标准液时,溶液蓝色恰好褪去且半分钟内不复原,说明到达滴定终点;
$\frac{226.25cV}{m}$.
点评 本题考查物质制备,为高考常见题型,涉及离子检验、方程式的计算、氧化还原反应等知识点,明确反应原理、离子检验方法、方程式的计算方法等知识点是解本题关键,侧重考查学生对实验操作及评价、化学反应原理的掌握及应用等能力,知道各个装置的作用及可能发生的反应,题目难点中等.


 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 四氯化碳-非电解质 氯化银-强电解质 碳酸-弱电解质 | |
| B. | NO2-酸性氧化物 CuO-碱性氧化物 Al2O3-两性氧化物 | |
| C. | 冰醋酸、纯碱、芒硝、生石灰分别属于酸、碱、盐、氧化物 | |
| D. | 碘酒、淀粉溶液、水雾、纳米材料均为胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
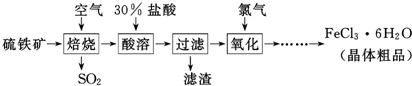

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
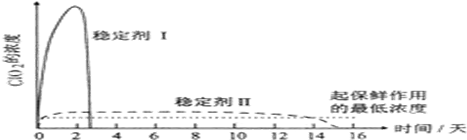
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
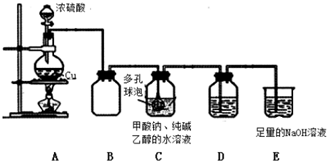
| 假 设 | 操 作 | 现 象 | 原 理 |
| Na2S2O4为强碱弱酸盐,其溶液为碱性. | 取少量溶液于试管中,滴加 ②紫色石蕊试液 | 溶液变成蓝色 | S2O42-水解,使溶液成碱性 |
| ①Na2S2O4具有还原性 | 取少量溶液于试管中,滴加过量新制氯水,再滴加 BaCl2 溶液 | 有白色沉淀生成 | 该反应的离子方程式依次为:③4H2O+S2O42-+3Cl2=2SO42-+6Cl-+8H+,④Ba2++SO42-=BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com