
【题目】用KMnO4氧化一定体积密度为1.19g/cm3 , 溶质质量分数为36.5%的 盐酸.反应方程式如下:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
(1)用双线桥法分析该反应(只需标出电子得失的方向和数目)
(2)15.8g KMnO4参加反应能消耗多少摩尔HCl?
(3)产生的Cl2在标准状况下的体积为多少升?
【答案】
(1)解:反应中高锰酸钾为氧化剂,浓盐酸为还原剂,Mn元素的化合价+7→+2,和Cl元素的化合价﹣1→0,反应中氧化剂和还原剂得失电子数目相等,则转移电子数为10e﹣,所以双线桥法可表示为: 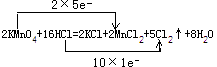 ;
;
故答案为: 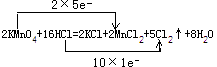
(2)解:设参加反应的HCl的物质的量为n,则:
2KMnO4 | + | 16HCl | = | 2KCl | + | 2MnCl2 | + | 5Cl2↑ | + | 8H2O |
2×158 | 16 | |||||||||
15.8g | n |
n= ![]() =0.8mol
=0.8mol
答:15.8g KMnO4参加反应能消耗0.8molHCl
(3)解:设生成氯气的物质的量为a,则:
2KMnO4 | + | 16HCl | = | 2KCl | + | 2MnCl2 | + | 5Cl2↑ | + | 8H2O |
2×158 | 5 | |||||||||
15.8g | a |
所以a= ![]() =0.25mol,
=0.25mol,
故生成标况下氯气的体积为0.25mol×22.4L/mol=5.6L,
答:标况下生成氯气的体积为5.6L
【解析】(1)反应中高锰酸钾为氧化剂,浓盐酸为还原剂,根据Mn元素的化合价+7→+2,和Cl元素的化合价﹣1→0,标出电子的转移方向和数目;(2)根据方程式计算需要HCl的物质的量;(3)据方程式计算生成氯气的物质的量,再根据V=22.4n计算生成氯气的体积.


科目:高中化学 来源: 题型:
【题目】从晶体与非晶体的角度分析,普通玻璃和水晶的根本区别是( )
A.外形不一样
B.普通玻璃的基本构成粒子无序排列,水晶的基本构成粒子呈周期性有序排列
C.水晶有固定的熔点,普通玻璃无固定的熔点
D.水晶可用于能量转换,普通玻璃不能用于能量转换
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.凡是放热反应的发生均无需加热
B.凡是需要加热后才能发生的反应是吸热反应
C.伴有能量变化的物质变化都是化学变化
D.物质发生化学反应都伴随着能量变化
查看答案和解析>>
科目:高中化学 来源: 题型:
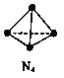
【题目】N4分子结构为正四面体(如图所示)。已知:断裂N4(g)中1 molN-N键吸收193kJ能量,形成N2(g)中1 mol N![]() N放出941 kJ能量。下列说法正确的是
N放出941 kJ能量。下列说法正确的是
A. N4(g)比N2(g)更稳定
B. N4(g)=2N2(g) △H=+724kJmol-1
C. 形成1 mol N4(g)中的化学键放出193 kJ的能量
D. lmolN2(g)完全转化为N4(g),体系的能量增加362kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应 SiO2(s)+C(s)+N2(g)![]() Si3N4(s)+CO(g)(未配平)△H <0,下列叙述正确的是
Si3N4(s)+CO(g)(未配平)△H <0,下列叙述正确的是
A. 该反应的氧化剂为N2,还原产物为CO
B. 增加焦炭的用量,生成氮化硅的反应速率增大
C. 反应中每生成0.1 mol Si3N4转移的电子为1.2 mol
D. 反应的平衡常数可表示为K=c(CO)/c(N2),升高温度K减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于苯的硝化反应,下列说法不正确的是( )
A.浓硫酸起了催化剂、吸水剂的作用
B.加热50-60℃通常通过水浴来实现
C.由于苯和硝酸都易挥发,所以通常需要加冷凝装置
D.纯净的硝基苯为深黄色比水重的液体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知31g白磷(P4)变为31g红磷(P)时释放能量。上述变化属于__变化(填“物理”或“化学”);稳定性白磷__红磷(填“>”或“<”);
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com