
锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水。当生成1 mol硝酸锌时,被还原的硝酸的物质的量为( )
A.2 mol B.1 mol C.0.5 mol D.0.25 mol
 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案科目:高中化学 来源: 题型:
在372K时,把0.5molN2O4通入体积为5L的真空密闭容器中,立即出现红棕色。反应进行到2s时,NO2的浓度为0.02mol/L。在60s时,体系达到平衡,此时容器内的压强为开始时压强的1.6倍。下列说法正确的是 高 考 资 源 网
A 前2s 以N2O4浓度变化表示的平均反应速率为0.01mol/(L.S)
B 在2s时体系内的压强为开始时的1.1倍
C 在平衡体系内含有N2O4 0.25mol D 平衡时N2O4的转化率为60%
查看答案和解析>>
科目:高中化学 来源: 题型:
能说明氯的非金属性比硫强的事实是
A.氯气与氢气反应生成氯化氢,而硫与氢气反应生成硫化氢
B.向硫化氢的水溶液中通入氯气可得到淡黄色的硫
C.氯气能与水反应而硫不能
D.氯原子最外电子层上有7个电子而硫最外电子层上有6个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法错误的是( )。
A.含有共价键的化合物一定是共价化合物 B.在共价化合物中一定含有共价键
C.含有离子键的化合物一定是离子化合物 D.双原子单质分子中的共价健一定是非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
结合短周期元素的性质用化学用语回答下列问题:
(1)与水反应最剧烈的金属是_____________。写出反应的离子方程式为_____________。(2)与水反应最剧烈的非金属单质是_____________。写出反应的化学方程式为_____________。
(3)最稳定的气态氢化物的化学式是_____________。
(4)除稀有气体外,原子半径最大的元素是_____,它与原子半径最小的元素形成的化合物属于 (离子、共价)化合物。
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学研究性学习小组对电解质溶液作如下的归纳总结:(均在常温下)
①常温下,pH=1的强酸溶液,加水稀释后,溶液中各离子的浓度一定降低
②pH=2的盐酸与pH=1的盐酸,c(H+)之比为2∶1
③25 ℃时,AgCl固体在等体积、等物质的量浓度的NaCl、CaCl2溶液中的溶解程度不同
④NH4HSO4溶液中滴加NaOH溶液至溶液pH=7,则c(Na+)=2c(SO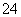 )
)
⑤已知醋酸电离平衡常数为Ka;醋酸根水解常数为Kh;水的离子积为Kw,则三者关系为:Ka·Kh=Kw
⑥甲、乙两溶液都是强电解质,已知甲溶液pH是乙溶液pH的两倍,则甲乙两溶液等体积混合,混合液pH可能等于7
其归纳正确的是( )
A.全部 B.③⑤⑥
C.④⑤⑥ D.①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
向足量H2SO4溶液中加入100 mL 0.4 mol·L-1 Ba(OH)2溶液,放出的热量是5.12 kJ。如果向足量Ba(OH)2溶液中加入100 mL 0.4 mol·L-1盐酸时,放出的热量为2.2 kJ。则Na2SO4溶液与BaCl2溶液反应的热化学方程式为 ( )。
A.Ba2+(aq)+SO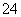 (aq)===BaSO4(s) ΔH=-2.92 kJ·mol-1
(aq)===BaSO4(s) ΔH=-2.92 kJ·mol-1
B.Ba2+(aq)+SO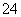 (aq)===BaSO4(s) ΔH=-18 kJ·mol-1
(aq)===BaSO4(s) ΔH=-18 kJ·mol-1
C.Ba2+(aq)+SO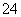 (aq)===BaSO4(s) ΔH=-73 kJ·mol-1
(aq)===BaSO4(s) ΔH=-73 kJ·mol-1
D.Ba2+(aq)+SO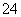 (aq)===BaSO4(s) ΔH=-0.72 kJ·mol-
(aq)===BaSO4(s) ΔH=-0.72 kJ·mol-
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
①氯气的性质活泼,它与氢气混合后立即发生爆炸
②实验室制取氯气时,为了防止环境污染,多余的氯气可以用氢氧化钙溶液吸收
③新制氯水的氧化性强于久置氯水
④检验HCl气体中是否混有Cl2方法是将气体通入硝酸银溶液
⑤除去HCl气体中的Cl2,可将气体通入饱和食盐水
A.①②③ B.②③④ C.③ D.③⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com