
| A. | S2-离子的结构示意图: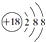 | B. | H2O2的电子式: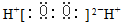 | ||
| C. | CO2的比例模型: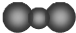 | D. | 有8个质子、10个中子的核素:188O |
分析 A.硫离子的核电荷数为16,不是18;
B.双氧水为共价化合物,不存在阴阳离子;
C.二氧化碳分子中,碳原子的原子半径大于氧原子;
D.质量数=质子数+中子数,元素符号的左上角为质量数、左下角为质子数.
解答 解:A.硫离子的核电荷数为16,最外层达到8电子稳定结构,硫离子正确的离子结构示意图为: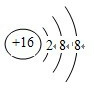 ,故A错误;
,故A错误;
B.双氧水为共价化合物,分子中存在两个氧氢键和一个O-O键,双氧水的电子式为 ,故B错误;
,故B错误;
C.二氧化碳分子中含有两个碳氧双键,碳原子的相对体积大于氧原子,其正确的比例模型为: ,故C错误;
,故C错误;
D.有8个质子、10个中子的核素的质量数为18,其表示方法为:188O,故D正确;
故选D.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及比例模型、电子式、离子结构示意图、元素符号等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的规范答题能力.


科目:高中化学 来源: 题型:多选题
| A. | Na2O>Na2O2 | B. | Na2CO3>NaHCO3>H2CO3 | ||
| C. | Na2SO4•10H2O>Na2CO3•10H2O | D. | NaClO>NaCl>NaF |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将pH=4的醋酸溶液稀释后,H+浓度增大 | |
| B. | 常温下,0.01L pH=10的NaOH溶液加水稀释到10L,此时溶液的pH=7 | |
| C. | 改变条件使醋酸的电离平衡向右移动,醋酸的电离度一定增大 | |
| D. | 常温下0.1mol•L-1醋酸溶液的pH=a,加入适量的醋酸钠固体能使溶液pH=(a+1) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
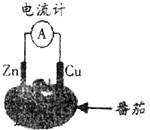
| A. | 电流由锌通过导线流向铜 | B. | 负极反应为Zn-2e-=Zn2+ | ||
| C. | 一段时间后,铜片质量会减少 | D. | 一段时间后,锌片质量会增加 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Al3+、NO3-、SO42- | B. | K+、Na+、CO32-、NO3- | ||
| C. | MnO4-、K+、SO42-、Na+ | D. | K+、Mg2+、SO32-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
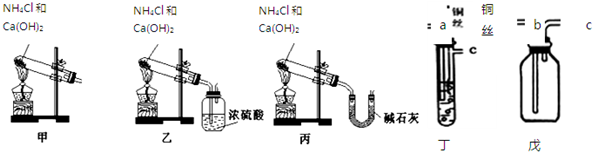
 2NH3.
2NH3.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com