
| A. | 澄清石灰水来吸收氯气:Cl2+OH-═Cl-+ClO-+H+ | |
| B. | 将金属Na加入冷水中:Na+2H2O═2Na++2OH-+H2↑ | |
| C. | 向稀硝酸中加入少量铁粉:3Fe+8H++2NO3═3Fe2++2NO↑+4H2O | |
| D. | 碳酸氢钙溶液中加入少量苛性钾溶液:OH-+Ca2++HCO3-=H2O+CaCO3↓ |
分析 A.氢氧化钙与氯气反应生成次氯酸钙、氯化钙和水;
B.离子方程式两边钠的质量不守恒;
C.铁粉少量,反应生成铁离子、一氧化氮气体和水;
D.苛性钾为氢氧化钾,氢氧化钾少量,反应生成碳酸氢钠、碳酸钙沉淀和水.
解答 解:A.澄清石灰水来吸收氯气,反应生成次氯酸钙、氯化钙和水,正确的离子方程式为:Cl2+2OH-═Cl-+ClO-+H2O,故A错误;
B.将金属Na加入冷水中,反应生成氢氧化钠和氢气,正确的离子方程式为:2Na+2H2O═2Na++2OH-+H2↑,故B错误;
C.向稀硝酸中加入少量铁粉,反应生成铁离子,正确的离子方程式为:Fe+4H++NO3-═Fe3++NO↑+2H2O,故C错误;
D.碳酸氢钙溶液中加入少量苛性钾溶液,离子方程式按照氢氧化钾的化学式书写,反应的离子方程式为:OH-+Ca2++HCO3-=H2O+CaCO3↓,故D正确;
故选D.
点评 本题考查了离子方程式的书写判断,为高考的高频题,题目难度中等,注意掌握离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等);D为易错点,注意反应物过量情况对生成物的影响.


科目:高中化学 来源: 题型:多选题
| A. | 28g氮气所含有的原子数目为NA | |
| B. | 常温常压下,32gO2含有的O原子数为NA | |
| C. | 1mol甲烷的质量与NA个甲烷分子的质量之和相等 | |
| D. | 标准状况下,22.4L 甲烷和乙炔的混合气体所含的分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
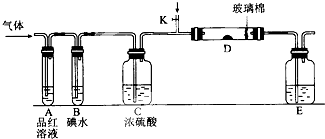 某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究S02和Cl2的性质.
某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究S02和Cl2的性质.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 晶体的世界丰富多彩,晶体的结构纷繁复杂.人教版课程标准高中教材《选修3》向我们展示了一些典型晶体的结构及性质的相关知识,如:干冰、冰、金刚石、石墨、钋、钾、镁、铜、NaCl、CsCl、CaF2.下图是一个立方晶胞图,请大家在上述所列物质范围内回答下列问题:
晶体的世界丰富多彩,晶体的结构纷繁复杂.人教版课程标准高中教材《选修3》向我们展示了一些典型晶体的结构及性质的相关知识,如:干冰、冰、金刚石、石墨、钋、钾、镁、铜、NaCl、CsCl、CaF2.下图是一个立方晶胞图,请大家在上述所列物质范围内回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知如图装置的甲、乙两室内装入液体的体积相同.请回答下列问题:
已知如图装置的甲、乙两室内装入液体的体积相同.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c (H+)<c (OH-) | B. | c (HX )<c (X-) | ||
| C. | c (X-)+c(HX )=2c (Na+) | D. | c (X-)-c (HX)═2(c( OH-)-c (H+)) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com