
科目:高中化学 来源:2014-2015福建省四地六校高二下学期第一次联考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.离子化合物中可能含有共价键,但不一定含有金属元素
B.分子中一定含有共价键
C.非极性分子中一定存在非极性键
D.极性分子中一定不存在非极性键
查看答案和解析>>
科目:高中化学 来源:2014-2015云南省高一3月月考化学试卷(解析版) 题型:选择题
下列物质中,不能通过单质间直接化合得到的是
A.FeCl3 B.FeI3 C.Na2O2 D.RbCl
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西省宝鸡市高一4月月考化学试卷(解析版) 题型:选择题
现有下列短周期元素性质的数据:下列关于表中11种元素的说法正确的是
元素 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |
原子半径(10-10m) | - | 0.37 | 0.74 | 0.75 | 0.77 | 0.82 | 0.99 | 1.10 | 1.52 | 1.60 | 1.86 |
最高或最低化合价 | 0 | +1 | +5 | +4 | +3 | +7 | +5 | +1 | +2 | +1 | |
-2 | -3 | -4 | -1 | -3 |
A.上表中11种元素中形成的非金属单质都有非极性共价键
B.②⑨处于同一周期,④⑧处于同一主族
C.上表中11种元素中最高价氧化物对应的水化物中⑦号酸性最强
D.⑥原子结构示意图为: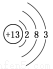
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西省宝鸡市高一4月月考化学试卷(解析版) 题型:选择题
下列分子中所有原子都满足最外层8电子稳定结构的是
A.六氟化氙(XeF6) B.次氯酸(HClO)
C.二氧化碳(CO2) D.三氟化硼(BF3)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市海淀区高三一模理综化学试卷(解析版) 题型:选择题
某温度下,将6 mol CO2和8 mol H2 充入2 L密闭容器中发生反应CO2(g) +3H2(g)  CH3OH(g) + H2O(g) ΔH < 0,容器中H2 的物质的量随时间的变化关系如图中的实线所示。图中虚线表示仅改变某一反应条件时,H2的物质的量随时间的变化关系。下列说法正确的是
CH3OH(g) + H2O(g) ΔH < 0,容器中H2 的物质的量随时间的变化关系如图中的实线所示。图中虚线表示仅改变某一反应条件时,H2的物质的量随时间的变化关系。下列说法正确的是
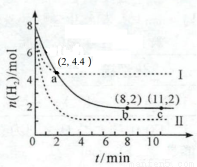
A.曲线Ⅰ对应的条件改变可能降低温度
B.曲线Ⅱ对应的条件改变可能是充入氦气
C.该温度下,此反应的化学平衡常数的数值为0.5
D.从反应开始至a 点,ν(CO2) = 0.6 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东湛江高三第二次模拟考试理综化学试卷(解析版) 题型:实验题
(16分)某实验小组模拟“侯氏制碱法”制纯碱,并进行以下探究:
(1)检验纯碱样品中是否混有NaHCO3,请选择下列装置设计实验,并完成下表:

选择的装置 (填编号) | 实验现象 | 实验结论 |
样品含 NaHCO3 |
(2)测定该纯碱样品的纯度:称取m1g样品,置于小烧杯中,加水溶解,滴加足量CaCl2溶液。将反应混和物过滤、 (填操作)、干燥、称量为m2g。该纯碱样品的纯度为 。
(3)该小组同学在0.1 mol/L NaHCO3溶液中滴加酚酞溶液1滴,溶液没有什么变化,但加热后显淡红色,加热较长时间后冷却,红色不褪去。为探究原因,进行了下列实验:
实验1: 加热0.1 mol/L NaHCO3溶液,测得溶液pH变化如下表
温度(℃) | 10 | 20 | 30 | 50 | 70 | 80 | 100 |
pH | 8.3 | 8.4 | 8.5 | 8.9 | 9.4 | 9.6 | 10.1 |
但当温度恢复到10 ℃,测得溶液pH=9.8。
实验2:加热0.1 mol/L NaHCO3溶液,将产生的气体通入澄清石灰水,澄清石灰水变浑浊。
①用离子方程式表示0.1 mol/L NaHCO3溶液中存在的平衡(除水电离平衡外) 、
________________。这两个平衡以__________为主。
②结合实验1、2分析,加热0.1 mol/L NaHCO3溶液,pH增大的原因可能是_____________(答一条)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省天水市高三下学期二模考试理综化学试卷(解析版) 题型:实验题
(14分)铝热反应是铝的一个重要性质。某校化学兴趣小组同学,取磁性氧化铁在如图实验装置进行铝热反应,冷却后得到“铁块”混合物。

(1)取反应后的“铁块”研碎取样称量,加入如图装置滴入足量NaOH溶液充分反应,测量生成气体体积。试回答下列问题:
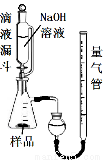
①该实验的实验目的是:测量样品中 的百分含量(填物质名称)。
②量气管的量具部分是一个中学实验常见量具改装而成,该仪器的名称为 。
③量气管在读数时调节左右管液面相平之前的步骤是________ _。
④装置中使用带平衡管的滴液漏斗代替普通分液漏斗,除了可以平衡压强让液体顺利滴入锥形瓶之外还可以起到降低实验误差的作用。如果装置使用分液漏斗,测量出的该物质百分含量将会 (填“偏大”或“偏小”)。
(2)另称取“铁块”样品溶于盐酸,向其中滴加KSCN溶液,溶液没有出现血红色。为测定该实验所得 “铁块”的成分,实验流程如图所示。

几种氢氧化物开始沉淀和完全沉淀的pH如下表所示。
Fe2+ | Fe3+ | Al3+ | Mg2+ | |
开始沉淀时的pH | 7.5 | 2.8 | 4.2 | 9.6 |
沉淀完全时的pH | 9.0 | 4.0 | 5 | 11 |
①试剂A应选择 ,试剂B应选择 。(填序号)
A.稀盐酸
B.氧化铁
C.H2O2溶液
D.氨水
E.MgCO3固体
②灼烧完全的标志是 。
③若最终红色粉未M的质量为12.0 g,则该“铁块”中铁的百分含量是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市丰台区高三第二次模拟理综化学试卷(解析版) 题型:实验题
(14分)硫是一种生命元素,组成某些蛋白质时离不开它。SO2是硫的一种重要氧化物,为探究SO2的性质,某化学兴趣小组的同学设计了如下系列实验:
(1)为验证SO2具有还原性。将SO2气体通入溴水中,溴水褪色。写出反应的化学方程式 。
(2)已知SO2与Na2O2的反应为进一步探究Na2O2与SO2的反应,用如图所示装置进行实验。
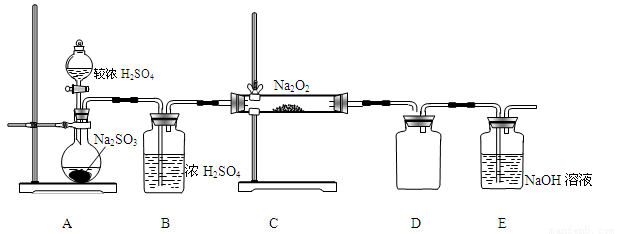
①写出A中反应的化学方程式 。
②B装置的作用是 。
③在F处检验到有O2生成,据此甲同学认为Na2O2与SO2发生了反应,反应的化学方程式为 。
④乙同学认为Na2O2与SO2反应除生成Na2SO3和O2外,还有Na2SO4生成,为检验是否有Na2SO4生成,他们设计了如下实验方案。
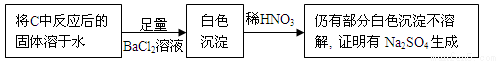
上述方案 (“合理”或“不合理”),简要说明理由 。
⑤E装置中溶液呈碱性,为检验吸收液中其他阴离子,完成下列实验方案。
实验步骤 | 实验现象 | 实验结论 |
取少量吸收液于试管中滴加BaCl2溶液至过量 | 白色浑浊 | |
固体部分溶解,产生气泡 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com