
【题目】设NA表示阿伏加德罗常数的值,下列说法正确的是 ( )
A.5.6 g Fe和足量的盐酸完全反应失去电子数为0.3 NA
B.常温常压下,200 g质量分数为17% 的H2O2溶液中含氧原子数目为NA
C.5.4g铝与足量NaOH溶液反应电子转移数为0.6NA
D.标况下,4.48L的水中含有H2O分子的数目为0.2NA
【答案】C
【解析】
A.5.6gFe的物质的量为:![]() =0.1mol,0.1mol Fe与足量盐酸反应生成氯化亚铁,失去0.2mol电子,即失去电子数为0.2NA,故A错误;
=0.1mol,0.1mol Fe与足量盐酸反应生成氯化亚铁,失去0.2mol电子,即失去电子数为0.2NA,故A错误;
B.200g质量分数为17%的H2O2溶液中,双氧水的质量为:200g×17%=34g,双氧水的物质的量为:![]() =1mol,含有2mol O原子,由于水分子中也含有氧原子,则该溶液中含氧原子数目大于2NA,故B错误;
=1mol,含有2mol O原子,由于水分子中也含有氧原子,则该溶液中含氧原子数目大于2NA,故B错误;
C.5.4g铝的物质的量为:![]() =0.3mol,铝与足量NaOH溶液反应的离子方程式为: 2Al +2OH-+2H2O=2AlO2-+3H2↑,根据关系式2Al
=0.3mol,铝与足量NaOH溶液反应的离子方程式为: 2Al +2OH-+2H2O=2AlO2-+3H2↑,根据关系式2Al![]() 6e-可知,0.3mol铝参与该反应时转移了0.3mol
6e-可知,0.3mol铝参与该反应时转移了0.3mol![]() 2=0.6mol电子,即电子转移数为0.6NA,故C正确;
2=0.6mol电子,即电子转移数为0.6NA,故C正确;
D.标况下水不是气体,不能使用标况下的气体摩尔体积计算,故D错误;
故选C。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】![]() 广泛存在于天然气等燃气及废水中,热分解或氧化
广泛存在于天然气等燃气及废水中,热分解或氧化![]() 有利于环境保护并回收硫资源。
有利于环境保护并回收硫资源。
(1)Binoist等进行了![]() 热分解实验:
热分解实验:![]() ,开始时,
,开始时,![]() 与
与![]() 的体积比为1:19.在压强为
的体积比为1:19.在压强为![]() 下测得在三种不同温度下
下测得在三种不同温度下![]() 的转化率如图1所示.
的转化率如图1所示.
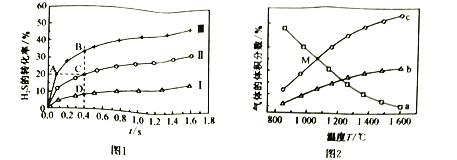
![]() 分解反应的
分解反应的![]() ______________(填“>”或“<”)0,A、B、C、D四点中:
______________(填“>”或“<”)0,A、B、C、D四点中:![]() 最大的是__________________,
最大的是__________________,![]() 最大的是___________,容器中
最大的是___________,容器中![]() 的分压由大到小的关系是__________________。
的分压由大到小的关系是__________________。
(2)当![]() 与
与![]() 混合,在
混合,在![]() 及不同温度下反应达平衡时
及不同温度下反应达平衡时![]() 及
及![]() 的体积分数如图2所示。图中b表示的物质是___________,M点时,反应
的体积分数如图2所示。图中b表示的物质是___________,M点时,反应![]() 的平衡常数
的平衡常数![]() ____________________
____________________![]() (
(![]() 为以分压表示的平衡常数,保留两位小数)
为以分压表示的平衡常数,保留两位小数)
(3)用氯气除去废水中![]() 的反应为
的反应为![]() ,该反应的可能机理如下:
,该反应的可能机理如下:
a.![]() 慢 b.
慢 b.![]() 快
快
![]() 快
快 ![]() 慢
慢
![]() 快
快 ![]() 快
快
c.![]() 慢 d.
慢 d.![]() 快
快
![]() 快
快 ![]() 慢
慢
①机理a的中间体为______________________。
②已知![]() ,
,![]() 为正反应速率,k为速率常数,上述机理中与该速率方程一致的是_________________________(填字母)。
为正反应速率,k为速率常数,上述机理中与该速率方程一致的是_________________________(填字母)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷(As)是第四周期ⅤA族元素,可以形成As2O3、As2O5、H3AsO3、H3AsO4等化合物,有着广泛的用途。回答下列问题:
(1)画出砷的原子结构示意图____________。
(2)工业上常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H3AsO4和单质硫。写出发生反应的化学方程式________。该反应需要在加压下进行,原因是________。
(3)已知:As(s)+![]() H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+![]() O2(g)=H2O(l) ΔH2
O2(g)=H2O(l) ΔH2
2As(s)+![]() O2(g) =As2O5(s) ΔH3
O2(g) =As2O5(s) ΔH3
则反应As2O5(s) +3H2O(l)= 2H3AsO4(s)的ΔH =_________。
(4)298 K时,将20 mL 3x mol·L1 Na3AsO3、20 mL 3x mol·L1 I2和20 mL NaOH溶液混合,发生反应:AsO33(aq)+I2(aq)+2OH![]() AsO43(aq)+2I(aq)+ H2O(l)。溶液中c(AsO43)与反应时间(t)的关系如图所示。
AsO43(aq)+2I(aq)+ H2O(l)。溶液中c(AsO43)与反应时间(t)的关系如图所示。

①下列可判断反应达到平衡的是__________(填标号)。
a.溶液的pH不再变化
b.v(I)=2v(AsO33)
c. c (AsO43)/c (AsO33)不再变化
d. c(I)=y mol·L1
②tm时,v正_____ v逆(填“大于”“小于”或“等于”)。
③tm时v逆_____ tn时v逆(填“大于”“小于”或“等于”),理由是_____________。
④若平衡时溶液的pH=14,则该反应的平衡常数K为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外时同学设计如下实验装置测定水的组成。
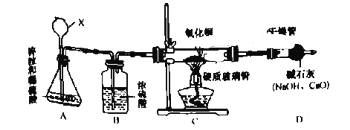
回答下列问题:
(1)仪器X的名称为____________。
(2)装置A中发生反应的化学方程式为______。
(3)当硬质玻璃管中固体由黑色转变为红色时,测得:①硬质玻璃管和其中固体的总质量反应后减少了1.6g;②干燥管的总质量在反应后增加了1.82g。由上述数据计算得出水中H、O元素的质量比为___(填最简整数比)。
(4)甲同学经分析认为:该装置存在缺陷,并对装置进行改进,其方法是________(假设生成的水完全被D中碱石灰吸收,装置内的水蒸气、CO2忽略不计)。
(5)乙同学查阅资料知:CuO被还原的过程中可能有Cn2O(红色)生成。若反应后硬质玻璃管中残留固体含有Cu2O,是否会影响该实验测定结果? _____________(填“影响”或“不影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿原酸是咖啡的热水提取液成分之一,结构简式如下图,关于绿原酸判断正确的是( )

A.1 mol绿原酸与足量NaHCO3溶液反应,生成3 mol CO2气体
B.1 mol绿原酸与足量溴水反应,最多消耗2.5 mol Br2
C.1 mol绿原酸与足量NaOH溶液反应,最多消耗4 mol NaOH
D.绿原酸水解产物均可以与FeCl3溶液发生显色反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药用有机物A为一种无色液体。从A出发可发生如下一系列反应:
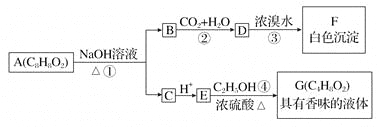
请回答:
(1)写出化合物F的结构简式:________________。
(2)写出反应①的化学方程式:__________________________________________。
(3)写出反应④的化学方程式:___________________________________________。
(4)有机物A的同分异构体很多,其中属于羧酸类的化合物,且含有苯环结构的有________种。
(5)E的一种同分异构体H,已知H可以和金属钠反应放出氢气,且在一定条件下可发生银镜反应。试写出H的结构简式:_________________________________。E的另一种同分异构体R在一定条件下也可以发生银镜反应,但不能和金属钠反应放出氢气。试写出R的结构简式:_____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一。
(1)基态O原子核外电子排布式为_______,基态Fe2+核外未成对电子数为_______,基态P原子核外占据最高能级的电子云轮廓图为_________形;
(2)比较大小(填“大于”、“小于”或“等于”):
①沸点:NH3_____PH3 ;②第一电离能:I1(P)_____I1(O)。
(3)PO43的空间构型是______,P原子的杂化形式为______,在1molPO43中含σ键______个。
(4)Li2O的晶胞如图所示(其中白球代表Li,黑球代表O)。已知晶胞参数为0.4665 nm,阿伏加德罗常数的值为NA,则Li2O的密度为______g·cm3(列出计算式即可)。
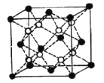
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中学化学中常用于混合物的分离和提纯的装置
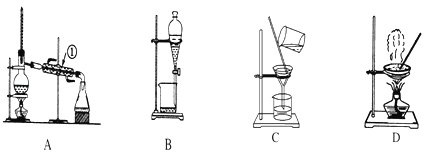
某化学兴趣小组利用以上装置,按以下实验方案,采取步骤(1)(2)(3)(4)等四步操作从海洋动物中提取具有抗肿瘤活性的天然产物。(已知甲苯和甲醇均为有机溶剂,有机物大多能互溶)
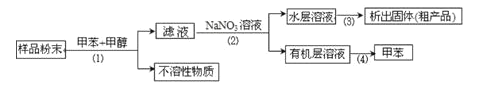
(1)装置A中仪器①的作用是________,使用装置A在流程中所对应的是________(填“操作(1)”“操作(2)”“操作(3)”或“操作(4)”,下同)。
(2)使用装置B在流程中所对应的是________在该操作中,振荡仪器时,为了避免因液体挥发而导致内部气压过大,还应进行的操作是________(填写具体的操作方法)。
(3)使用装置C在流程中所对应的是________,若所得沉淀不溶于水且需要洗涤,则洗涤的具体操作是________。
(4)使用装置D在流程中所对应的是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com