
����Ŀ��ͨ���Ѳ�1 molij��ѧ�������յ��������ɸû�ѧ���ļ��ܣ���֪���ֻ�ѧ���ļ������£�
��ѧ�� | N��H | N��N | O=O | N��N | O��H |
����(kJ��mol��1) | 386 | 167 | 498 | 946 | 460 |
��1���������۷ɴ��ij������������(N2H4����̬)Ϊȼ�ϣ�����������(��̬)��ȼ�գ�����N2(��̬)��H2O(Һ̬)��1 mol����ȫȼ��ʱ�ų�������Ϊ________��
��2����-����ȼ�ϵ����һ�ּ���ȼ�ϵ�أ��������Һ��20%��30%��KOH ��Һ����-����ȼ�ϵ�طŵ�ʱ�������ĵ缫��Ӧʽ��______________________________________��
��3����֪N60������ÿ��Nԭ�Ӿ��Ե��������������ԭ�ӣ���N60���ӽṹ��ÿ����ԭ�����γ�8�����ӵ��ȶ��ṹ�����Ʋ�1��N60�Ľṹ����________��N��N����
���𰸡���1��577 kJ��2��O2��4e����2H2O=4OH����3��90
��������
���������
��1��N2H4ȼ�յĻ�ѧ����ʽΪN2H4��g��+O2��g���TN2��g��+2H2O��g������H=��Ӧ����ܼ���-��������ܼ���=167 kJ��mol-1+386 kJ��mol-1��4+498 kJ��mol-1-946 kJ��mol-1-460 kJ��mol-1��4=-577 kJ��mol-1��N2H4ȼ�յ��Ȼ�ѧ����ʽΪN2H4��g��+O2��g���TN2��g��+2H2O��g����H=-577 kJ��mol-1������1mol����ȫȼ��ʱ�ų�������Ϊ577 kJ���ʴ�Ϊ��577kJ��
��2���£�����ȼ�ϵ���У�O2�������ŵ磬����OH����
��3��N60������ÿ��Nԭ�Ӿ��Ե��������������ԭ�ӣ�������Ϊ������ԭ�ӹ��ã�1��N60�Ľṹ����N��N��������![]() ��
��


 ��ְٷְټ���ϵ�д�
��ְٷְټ���ϵ�д� �����ƻ���ĩ��̶�100��ϵ�д�
�����ƻ���ĩ��̶�100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A��B��C��D���ֽ������±���װ�ý���ʵ�顣
װ�� |
|
|
|
���� | ���۽���A �����ܽ� | C���� ������ | A������ ����� |
����ʵ������ش��������⣺
��1��װ�ü��и����ĵ缫��Ӧʽ��____________________________________��
��2��װ�����������ĵ缫��Ӧʽ��_____________________________________����Һ��Cu2����______���ƶ�(����B������C��)��
��3����װ�ñ�������3.36L����״��������ʱ����·��ת�Ƶĵ�����ĿΪ____________��
��4�����ֽ��������ǿ������˳����__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ŀǰ�������嵥�ʵķ�����Ҫ��ˮ����������ȡ���ȡ�ij��ȤС��ͨ���������������������·����Ӹ������Һ������0.27%���л����ӷ���Br2��

��1������X����Ҫ����Ҫ��������Ϊ ��������ʹ��ǰ���©�����鷽��Ϊ ��
��2������ȡʱ����20%��NaOH��Һ�������ӷ���ʽΪ ��
��3������ȡ����ˮ���ữʱ���軺������Ũ���ᣬ�����ñ�ˮԡ��ȴ��ԭ���� ��
��4����Ĵ�ͳ��������Ϊ�Ȳ����������������ÿ���ˮ������Br2�������봫ͳ������ȣ���ȡ�����ŵ��� ��
��5���ҹ���ˮ�����ŷű��涨����ˮ�б��ӵĺ������ó���1.00mg��L�D1��ʵ���ҿ���һ��Ũ�ȵ���ˮ�ⶨij��ˮ�б��ӵĺ�������ԭ�����£�

���������Ӧ��ʵ�鲽�裺
����1��ȷ��ȡ25.00mL�����ˮ��250mL��ƿ�С�
����2����4.5mL 0.02mol��L�D1��ˮѸ�ټ��뵽��ƿ�У�����ƿ������
����3����ƿ��������ƿ�м��������0.1mol��L�D1 KI��Һ����
����4�� ������0.01mol��L�D1 Na2S2O3����Һ�ζ����յ㣬���� Na2S2O3��Һ15mL����Ӧԭ����I2+2Na2S2O3=2NaI+Na2S4O6����
����5����ʵ�鲽��1��4�ظ�2�Ρ�
���÷�ˮ�б��ӵĺ���Ϊ mg��L�D1��
������3������ʱ��ϳ������õķ�ˮ�б��ӵĺ��� ���ƫ�ߡ�����ƫ�͡�����Ӱ�족����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ȼ�����SO2Cl2����һ����ɫҺ�壬��Ҫ�����л����������Ȼ��ȡ����۵�Ϊ-54.1��.�е�Ϊ69.2���������±Ƚ��ȶ��������ֽ⣬��ˮ���ҷ�Ӧ������������ᡣ
��1���Ʊ���ʵ���ҿ�����SO2��Cl2������װ����ȡ����SO2Cl2�����з�������Һ��������ã�����֪SO2(g)+Cl2(g)![]() SO2Cl2(g) ��H��0
SO2Cl2(g) ��H��0
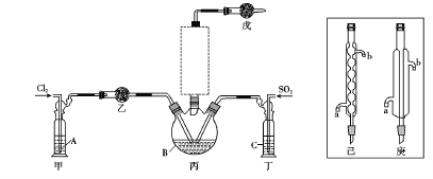
��������Ũ��������Ը��������ȡ�������÷�Ӧ�Ļ�ѧ����ʽΪ ����ҺAΪ ��
����ͼʵ����������������Ϊ ����Ӧװ��ͼ�������δ������������ ����������������������
���������װ�÷����ˮ�У���������ڶ��Ȼ��������ɣ���ԭ���� ��
�������й�˵��������� �����ţ���
a.�ҡ���װ����ͬ����ʵ���е�����Ҳ��ȫ��ͬ
b.�ס���װ��Ϊϴ��װ�ã�����������ij��Ӻ���
c.��װ����������Ҫ���еIJ����Ǽ��װ�õ�������
d.Ϊ��߷�Ӧ��������ʣ��ɿ��Ƽס���װ���в������ݵ��������
��2���ᴿ�����ռ����IJ�����м�ѹ����ѹ�����Ŀ���� ��
��3���ⶨ��ȡ1.00g�����Һ�壬С�ĵ���ȫ����ˮ�������õ���Һ�м��������Ȼ�����Һ��������ɳ���������Ϊ1.60g������������ɷ��ж��Ȼ����������ٷֺ���Ϊ %��
��4�����档���Ȼ���Ӧ���������������ͨ�����õĿⷿ�������ú��Ի�ɫ����ԭ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ѧ��ѡ��5:�л���ѧ���л���A��F������ת����ϵ��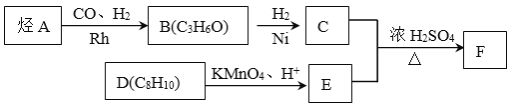
��֪����
�ں˴Ź���������ʾC�ķ����к���4�ֲ�ͬ��ѧ��������ԭ�ӣ��ҷ����֮��Ϊ3:2:2:1��
��F�������������б����ϵ�һ�����ֻ�����֡�
��1��A�ķ���ʽ�� ����Ҫ��;�� ��дһ�֣���
��2������B�й����ŵij��÷����� ��
��3��D���ʵ�����Ϊ ��
��4��C+E��F�Ļ�ѧ����ʽ�� ��
��5��X��E��Ϊͬ���칹�壬��X���������ʣ�����������X�� �֡�
�ٽӴ�NaHCO3�ж�����̼���������
����������Һ��������������
��1Ħ��X�������Ʒ�Ӧ��1Ħ�����������
��6��Y��EҲ��Ϊͬ���칹�壬����������������ֻ��һ�ֹ����ţ��ұ����ϵ�һ����ȡ����ֻ��һ�֣���Y�Ľṹ��ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����X��Y��Z��T��U���ֶ�����Ԫ�ء�X��Y��Z��Ԫ�������ڱ��е�λ��������ʾ����Ԫ�ص�ԭ������֮����41��X��T�ĵ����ڲ�ͬ�����·�Ӧ����������T2X(��ɫ����)��T2X2(����ɫ����)���ֻ����U������Z������ȼ��ʱ������ɫ���棬�������ˮ��Һ��ʹʯ����Һ��졣
X | |
Y | Z |
��1����Ԫ�صķ����ǣ�Z________��T________
��2��Yԭ�ӵĽṹʾ��ͼΪ____________________,U2X�ĵ���ʽ
��3��YX2��U2Y��Ӧ�Ļ�ѧ����ʽΪ____________________________��������������____________����������Ԫ����____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�Ǻϳ��л��߷��Ӳ���W������ͼ��

��֪�� 
�ش��������⣺��1��B�Ľṹ��ʽ��____ ____
��2��E�����������ŵĽṹ��ʽ��
��3��B��C��Ӧ����Ϊ_ _____ __
��4��д�����з�Ӧ�Ļ�ѧ����ʽ��
D��E��W:___________ __
C��������Һ��Ӧ��___________ ___
��5����������������E��ͬ���칹���� ��
�� �ɷ���������Ӧ �� ����NaHCO3��Һ����CO2 ������FeCl3��Һ��Ӧ����ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������и�װ��ͼ�������У��������

A��װ����������ⱥ��ʳ��ˮ��c�缫������������ʹʪ��ĵ���KI��ֽ����
B��װ�����������ռ�H2��NH3��Cl2��HCl��NO2
C��װ���������Ȳ�Ļ�ԭ��
D��װ���������ڸ���ռ������������ն���İ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ļ������ڹ�ũҵ�����������о�����ҪӦ�á���ش�����������
(1)���������г���N2H4��Ϊ����������ȼ����N2H4�백�����ƣ���һ�ּ������壬������ˮ����������N2H4��H2O���õ��뷽��ʽ��ʾN2H4��H2O�Լ��Ե�ԭ�� ��
��2���ں��������£�1 mol NO2������C������Ӧ:2NO2(g)+2C(s)![]() N2(g)+2CO2(g)�����ƽ��ʱNO2��CO2�����ʵ���Ũ����ƽ����ѹ�Ĺ�ϵ��ͼ��ʾ��
N2(g)+2CO2(g)�����ƽ��ʱNO2��CO2�����ʵ���Ũ����ƽ����ѹ�Ĺ�ϵ��ͼ��ʾ��
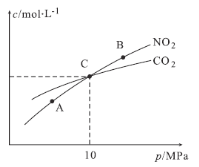
��A��B�����Ũ��ƽ�ⳣ����ϵ��Kc(A) Kc(B)�������������=������
��A��B��C������NO2��ת������ߵ��� ������A������B������C��������
������C��ʱ�÷�Ӧ��ѹǿƽ�ⳣ��Kp= ���г�����ʽ����������Kp����ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ����ѹ�����ʵ�����������
��3��������ĵ���ƽ�ⳣ��Ka=5.1��10-4��298K�����������ʺ���������ơ�
����֪298K ʱ��H2CO��Ka1=4.2��10-7 ��Ka2=5.61��10-11������2mol̼���Ƶ���Һ�м���1mol��HNO2������Һ��CO32-��HCO3-��NO2-������Ũ���ɴ�С�� ��
����10mL0.1mol/L����������Һ���뵽10mL0.1mol/L��ˮ����֪��25��ʱ��һˮ�ϰ���Ki= 1.8��10-5����,���������ҺΪ________��������������������������������������
��4��һ��ú̿������������Ԫ����CaSO4���γɹ̶���������������CO�ֻ���CaSO4������ѧ��Ӧ����ص��Ȼ�ѧ����ʽ���£�
��CaSO4��s��+CO��g��![]() CaO��s��+SO2��g��+CO2��g����H = +210.5kJmol-1
CaO��s��+SO2��g��+CO2��g����H = +210.5kJmol-1
��CaSO4��s��+ 4CO��g��![]() CaS��s��+ 4CO2��g�� ��H = -189.2kJmol-1
CaS��s��+ 4CO2��g�� ��H = -189.2kJmol-1
��ӦCaO(s)+3CO(g)+SO2(g) ![]() CaS(s)+3CO2(g) ��H= kJmol-1��
CaS(s)+3CO2(g) ��H= kJmol-1��
(5)H2S��������ˮ�γɵ���������һ�ֶ�Ԫ���ᣬ25��ʱ����0.10 mol��L-1H2S��Һ�У�ͨ��HCl��������NaOH�����Ե�����ҺpH����ҺpH��c(S2-)��ϵ��ͼ��ʾ(������Һ����ı仯��H2S�Ļӷ�)��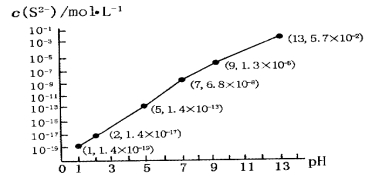
��pH=13ʱ����Һ�е�c(H2S)+c(HS-)=__________mol��L-1��
��ij��Һ��0.010 mol��L-1Fe2+��0.10 mol��L-1H2S������ҺpH=______ʱ��Fe2+��ʼ����������֪��KSP(FeS)=1.4��10-19��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com