
在一密闭容器中加入xmol的Na2O2和ymol的NaHCO3固体充分加热,下列有关加热后容器中残留固体成分和导出气体成分的说法正确的是![]()
A.若x=y,气体中只含有0.5x molO2,固体中含有2y molNa2CO3和y molNaOH![]()
B.若0.5y<x<y,气体中含有0.5y molH2O,固体中含有y molNaOH和y molNa2CO3![]()
C.若0.5y=x,气体中有0.5x molO2,固体中有y molNaOH和y molNa2CO3![]()
D.若x<0.5y,气体中含有(0.5y—x)molCO2,固体中含有(x+0.5y)molNa2CO3![]()
科目:高中化学 来源: 题型:阅读理解
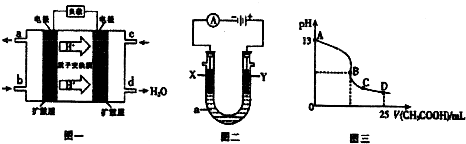
| 实验组 | 温度/K | 平衡浓度mol/L | ||
| CH3OH | CH3OCH3 | H2O | ||
| 1 | 403 | 0.01 | 0.2 | 0.2 |
| 2 | 453 | 0.02 | 0.3 | 0.4 |
| 0.2×0.2 |
| (0.01)2 |
| 0.3×0.4 |
| (0.02)2 |
| 0.2×0.2 |
| (0.01)2 |
| 0.3×0.4 |
| (0.02)2 |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
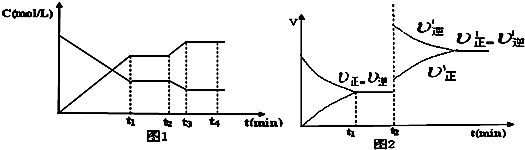
 3Z(g)△H<O
3Z(g)△H<O| c3(z) |
| c(x)?c2(y) |
| c3(z) |
| c(x)?c2(y) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
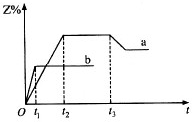 一密闭容器中加入相同物质的量的X和Y气体,发生反应:X(g)+Y(g)?3Z(g).分别在100℃和300℃反应时Z的体积分数Z%随时间t变化如图所示.已知在t3时改变了某一反应条件.则相关判断正确的是( )
一密闭容器中加入相同物质的量的X和Y气体,发生反应:X(g)+Y(g)?3Z(g).分别在100℃和300℃反应时Z的体积分数Z%随时间t变化如图所示.已知在t3时改变了某一反应条件.则相关判断正确的是( )查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com