
 (1)实验室用如图所示装置制备少量乙酸乙酯.
(1)实验室用如图所示装置制备少量乙酸乙酯. .试回答:
.试回答: +2Na→
+2Na→ +H2↑.
+H2↑. 分析 (1)实验室制备乙酸乙酯用乙醇和乙酸在浓硫酸作催化剂条件下加热反应生成,用饱和碳酸钠溶液吸收,分离互不相溶的液体,可用分液的方法分离,以此解答该题;
(2)根据结构简式来寻找出现的官能团;醇和羧酸均能和金属钠发生置换反应生成氢气.
解答 解:(1)①实验室制备乙酸乙酯用乙醇和乙酸在浓硫酸作催化剂条件下加热反应生成,反应的方程式为CH3COOH+CH3CH2OH $?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O,故答案为:CH3COOH+CH3CH2OH $?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;
②实验室用饱和碳酸钠溶液吸收,因乙酸乙酯不溶于饱和碳酸钠溶液,且饱和碳酸钠溶液可起到除去乙酸和乙醇的作用,故答案为:饱和Na2CO3溶液;
③分离乙酸乙酯时先将盛有混合物的试管充分振荡,让饱和碳酸钠溶液中和挥发出来的乙酸,使之转化为乙酸钠溶于水中,溶解挥发出来的乙醇;降低乙酸乙酯在水中的溶解度,静置分层后取上层得乙酸乙酯,故答案为:分液;
(2)①根据乳酸的结构简式可以看出其中含有的官能团为:羟基,羧基,故答案为:羟基;羧基;
②乳酸中的醇羟基和羧基均与金属钠反应,反应的化学方程式为 +2Na→
+2Na→ +H2↑,
+H2↑,
故答案为: +2Na→
+2Na→ +H2↑.
+H2↑.
点评 本题考查有机物的性质以及化学方程式的书写知识,注意官能团对物质性质的决定作用,可以根据所学知识进行回答,难度不大.


 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 达到化学平衡时,N2完全转化为NH3 | |
| B. | 一定条件下达到化学平衡时,N2、H2和NH3的物质的量浓度之比为1:3:2 | |
| C. | 单位时间内消耗a mol N2同时消耗2amol NH3,说明该反应已达到平衡状态 | |
| D. | 达到化学平衡时,正反应和逆反应速率相等,且都为零 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 请运用化学反应原理的相关知识研究碳及其化合物的性质.
请运用化学反应原理的相关知识研究碳及其化合物的性质.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯酚(C6H5OH)能跟NaOH溶液反应而乙醇不能 | |
| B. | 乙烯能发生加成反应而乙烷不能 | |
| C. | 甲苯能使KMnO4酸性溶液褪色而乙烷不能 | |
| D. | 苯在50℃~60℃时发生硝化反应而甲苯在30℃时即可 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯使酸性KMnO4溶液褪色 | |
| B. | 将苯滴入溴水中,振荡后水层接近无色 | |
| C. | 乙烯使溴水褪色 | |
| D. | 甲烷与氯气混合,光照一段时间后黄绿色变浅 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加热氧化银 | B. | 煅烧碳酸钙 | ||
| C. | 电解氯化钠溶液 | D. | 氯化镁与铝粉高温共热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙烯的结构简式可以表示为CH3CHCH2 | |
| B. | 用酒精可以将溴水中的溴萃取出来 | |
| C. | 乙烷、乙醇和乙酸都能发生取代反应 | |
| D. | 油脂都不能使酸性高锰酸钾溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 93.5L | B. | 95L | C. | 97.5L | D. | 98.5L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
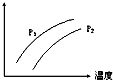 如图表示温度、压强对达平衡的可逆反应:2L(g)?2M(g)+N(g)△H>0的影响(P1<P2)图中y轴表示的意义是( )
如图表示温度、压强对达平衡的可逆反应:2L(g)?2M(g)+N(g)△H>0的影响(P1<P2)图中y轴表示的意义是( )| A. | 混合物中L的百分含量 | B. | 混合气体的密度 | ||
| C. | L的转化率 | D. | 混合气体的平均分子量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com