
日常生活中的许多现象与化学反应有关,下列现象与氧化还原反应无关的是( )
|
| A. | 铜铸塑像上出现铜绿 |
|
| B. | 铁制菜刀生锈 |
|
| C. | 大理石雕像被酸雨腐蚀毁坏 |
|
| D. | 铝锅表面生成致密的氧化膜 |
考点:
氧化还原反应.
专题:
氧化还原反应专题.
分析:
根据信息判断发生的化学反应,在反应中存在元素的化合价变化时则发生的反应为氧化还原反应,以此来解答.
解答:
解:A.金属铜和氧气、二氧化碳、水发生化合反应生成铜绿,该反应中有元素化合价的变化,所以属于氧化还原反应,故A不选;
B.铁在氧气、水存在时发生电化学腐蚀而生锈,该反应中有元素化合价的变化,所以属于氧化还原反应过程,故B不选;
C.酸雨腐蚀大理石雕像是因为碳酸钙能和酸反应,该反应中没有元素化合价的变化,所以不是氧化还原反应,属于复分解反应,故C选;
D.铝易被氧气氧化生成氧化铝,该反应中有元素化合价的变化,所以属于氧化还原反应,故D不选;
故选C.
点评:
本题考查生活中的氧化还原反应,明确发生的化学反应是解答的关键,难度不大.


科目:高中化学 来源: 题型:
某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.
实验编号 反应物 催化剂
① 10mL2% H2O2溶液 无
② 10mL5% H2O2溶液 无
③ 10mL5% H2O2溶液 1mL0.1mol•L﹣1FeCl3溶液
④ 10mL5% H2O2溶液+少量HCl溶液 1mL0.1mol•L﹣1FeCl3溶液
⑤ 10mL5% H2O2溶液+少量NaOH溶液 1mL0.1mol•L﹣1FeCl3溶液
(1)催化剂能加快化学反应速率的原因是 .
(2)常温下5% H2O2溶液的pH约为6,H2O2的电离方程式为 .
(3)实验①和②的目的是 .实验时由于没有观察到明显现象而无法得出结论.资料显示,通常条件下H2O2稳定,不易分解.为了达到实验目的,你对原实验方案的改进是 ).
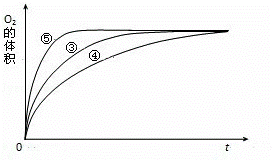
(4)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图.
分析上图能够得出的实验结论是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
铜和镁的合金4.6g完全溶于浓硝酸,若反应后硝酸被还原只产生 2.24L的 NO2气体和1.12L的N2O4气体(都已折算到标准状况),在反应后的溶液中,加入足量的氢氧化钠溶液,生成沉淀的质量为()
A. 9.02g B. 8.51g C. 8.00g D. 7.04g
查看答案和解析>>
科目:高中化学 来源: 题型:
下列电离方程式错误的是( )
|
| A. | K2CO3=2K++CO32﹣ | B. | KClO3=K++ClO3﹣ |
|
| C. | H2CO3⇌2H++CO32﹣ | D. | NaHCO3=Na++HCO3﹣ |
|
| E. | K2CO3=2K++CO32﹣ |
|
|
查看答案和解析>>
科目:高中化学 来源: 题型:
在强酸性溶液中能大量共存的离子组是( )
|
| A. | Ca2+、Na+、NO3﹣、CO32﹣ | B. | Mg2+、Cl﹣、NH4+、SO42﹣ |
|
| C. | K+、Cl﹣、HCO3﹣、NO3﹣ | D. | Ca2+、Na+、Fe2+、NO3﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是( )
|
| A. | 用小苏打治疗胃酸过多: |
|
| B. | 用食醋除去水瓶中的水垢: |
|
| C. | 漂白粉溶液中加入稀盐酸:H++ClO﹣=HClO |
|
| D. | 向澄清石灰水中通入过量的二氧化碳气体:Ca2++2OH﹣+CO2=CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
只用一种试剂就能鉴别Ba(NO3)2、Na2CO3、K2SO4三种溶液,该试剂是()
A. KNO3溶液 B. 稀H2SO4 C. NaOH溶液 D. Na2SO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
有如下合成路线,甲经二步转化为丙:

下列叙述错误的是( )
|
| A. | 物质丙能与浓硫酸加热发生消去反应 |
|
| B. | 甲和丙均可与酸性KMnO4溶液发生反应 |
|
| C. | 反应(1)需用铁作催化剂,反应(2)属于取代反应 |
|
| D. | 步骤(2)产物中可能含有未反应的甲,可用溴水检验是否含甲 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com