
| A. | 实验后剩余的钠粒,需要放回原试剂瓶中 | |
| B. | 自然界中钠只能以化合物的形式存在 | |
| C. | 钠的化学性质比较活泼,少量的钠可以保存在与钠不反应的煤油中 | |
| D. | 当钠与硫酸铜溶液反应时,有大量红色固体铜出现 |
分析 A、实验剩余的金属单质和非金属单质应放回原试剂瓶;
B、钠是非常活泼的金属;
C、钠的密度比煤油的大,且和煤油不反应;
D、钠和盐溶液反应时,先和水反应,生成的氢氧化钠再和盐反应.
解答 解:A、实验剩余的金属单质和非金属单质应放回原试剂瓶,即剩余的钠应放回原试剂瓶,故A正确;
B、钠是非常活泼的金属,极易和氧气、水等反应,故在自然界无钠单质,只能以化合态存在,故B正确;
C、钠的密度比煤油的大,且和煤油不反应,故保存在煤油中可以隔绝空气和水,故C正确;
D、钠和盐溶液反应时,先和水反应,生成的氢氧化钠再和盐反应,即不能置换出金属铜,故D错误.
故选D.
点评 本题考查了钠单质的有关化学性质和保存方法,难度不大,应注意的是钠只能保存在煤油或石蜡油中,不能保存在四氯化碳中.


科目:高中化学 来源: 题型:选择题
| A. | 若实验室发生火灾,应立即打开门窗(或排风扇)通风透气 | |
| B. | 实验结束后,用嘴吹熄酒精灯 | |
| C. | 皮肤上不慎沾上NaOH溶液,立即用盐酸冲洗 | |
| D. | 稀释浓硫酸时,将浓硫酸沿器壁慢慢注入水中,并不断的搅拌 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
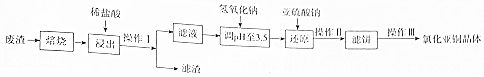
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
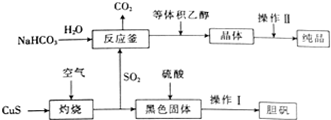 硫及其化合物在生产及生活中有着广泛的应用.
硫及其化合物在生产及生活中有着广泛的应用.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸、纯碱、石膏 | B. | 盐酸、烧碱、胆矾 | ||
| C. | HNO3、乙醇、氯化钠 | D. | H3PO4、熟石灰、苛性钾 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com