
 氮化铝(AlN)是一种人工合成的非氧化物陶瓷材料,可在温度高于1500℃时,通过碳热还原法制得.实验研究认为,该碳热还原反应分两步进行:①Al2O3在碳的还原作用下生成铝的气态低价氧化物X(X中Al与O的质量比为6.75:2);②在碳存在下,X与N2反应生成AlN.请回答:
氮化铝(AlN)是一种人工合成的非氧化物陶瓷材料,可在温度高于1500℃时,通过碳热还原法制得.实验研究认为,该碳热还原反应分两步进行:①Al2O3在碳的还原作用下生成铝的气态低价氧化物X(X中Al与O的质量比为6.75:2);②在碳存在下,X与N2反应生成AlN.请回答:分析 (1)依据X中Al与O的质量比为6.75:2计算物质的量之比得到化学式;
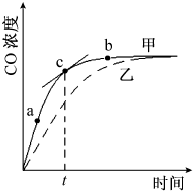
(2)①A、图象中可以得到单位时间内的浓度变化,反应速率是单位时间内物质的浓度变化;
B、c点处的切线的斜率是此时刻物质浓度除以此时刻时间为瞬时速率;
C、化学反应速率之比等于化学方程式计量数之比分析;
D、维持温度、容积不变,若减少N2的物质的量进行反应,平衡逆向进行,达到新的平衡状态;
②该反应只有在高温下才能自发进行,结合反应自发进行的判断依据是△H-T△S<0分析.
解答 解:(1)X中Al与O的质量比为6.75:2计算物质的量之比=$\frac{6.75}{27}$:$\frac{2}{16}$=0.25:0.125=2:1,化学式为:Al2O,
故答案为:Al2O;
(2)①A、图象中可以得到单位时间内的浓度变化,反应速率是单位时间内物质的浓度变化计算得到,从a、b两点坐标可求得从a到b时间间隔内该化学反应的平均速率,故A正确;
B、c点处的切线的斜率是此时刻物质浓度除以此时刻时间,为一氧化碳的瞬时速率,故B正确;
C、化学反应速率之比等于化学方程式计量数之比分析,3v(N2)=v(CO),故C错误;
D、维持温度、容积不变,若减少N2的物质的量进行反应,平衡逆向进行,达到新的平衡状态,平衡状态与原来的平衡状态不同,故D错误;
故答案为:CD;
②若温度不变,反应体系的压强减小为0.5p,平衡向气体体积增大的方向进行,平衡正向进行,N2的平衡转化率增大,平衡时CO的物质的量浓度增大,CO的物质的量浓度大于0.5c,小于c,故选B,
故答案为:>;B.
点评 本题考查了化学式计算书写、化学平衡影响因素分析判断,主要是图象分析应用,掌握基础是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | H2、I2、HI的浓度相等 | |
| B. | 混合气体密度恒定不变 | |
| C. | 混合气体的质量不再改变 | |
| D. | 1个I-I键断裂的同时,有2个H-I键断裂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过氧化钠是淡黄色固体,久置于空气中变成白色的氢氧化钠固体 | |
| B. | 过氧化钠中阴阳离子比例为1:2 | |
| C. | 用过氧化钠漂白织物、麦秆等日久又逐渐变成黄色 | |
| D. | Na2O与Na2O2都能和水反应生成碱,它们都是碱性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在水溶液里或熔融状态下能够导电的物质叫做电解质 | |
| B. | 微粒直径在10-9 m-10-7m之间的分散系为胶体 | |
| C. | 能够电离出氢离子的化合物叫酸 | |
| D. | 胶体区别于其他分散系的本质特征是具有丁达尔效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

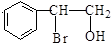 ,F分子中含有的含氧官能团名称是羟基、羧基(顺序可以颠倒).
,F分子中含有的含氧官能团名称是羟基、羧基(顺序可以颠倒). .
.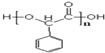 .
.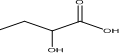 的合成线路:H2C=CHCH2CH3$\stackrel{HBrO}{→}$HOCH2CHBrCH2CH3→CH3CH2CHBrCOOH$\stackrel{NaOH(aq)△}{→}$CH3CH2CHOHCOOH.
的合成线路:H2C=CHCH2CH3$\stackrel{HBrO}{→}$HOCH2CHBrCH2CH3→CH3CH2CHBrCOOH$\stackrel{NaOH(aq)△}{→}$CH3CH2CHOHCOOH.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ③②① | C. | ②③① | D. | ②①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实 验 事 实 | 结 论 | |
| A | A、B两种有机物具有相同的相对分子质量和不同的结构 | A、B互为同分异构体 |
| B | 质量相同的A、B两种有机物完全燃烧生成质量相同的水 | A、B两有机物最简式相同 |
| C | A、B两种有机物结构相似具有相同的通式 | A、B互为同系物 |
| D | 分子式为C6H6的烃A既能使溴的CCl4溶液褪色,又能使酸性KMnO4溶液褪色 | A的结构简式可能是 CH2═CH-C≡C-CH═CH2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com