
【题目】请运用原电池原理设计实验,验证 Cu2+、Fe3+氧化性的强弱。请写出电极反应式。
(1)负极 __________________________
(2)正极 __________________________________
(3)并在方框内画出实验装置图,要求用烧杯和盐桥,并标出外电路中电子流向。________________________________
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案科目:高中化学 来源: 题型:
【题目】钛铁矿是铁和钛的氧化物矿物,成分可表示为FeTiO3(Ti为+4价)。钛白粉(TiO2)涂料、塑料、油墨、造纸行业具有广泛的用途,制备流程如图:

(1)钛铁矿与硫酸反应时可表示为FeTiO3+H2SO4→TiOSO4+X+H2O,其中X的化学式为 ______,该反应为______ (填“氧化还原反应”或“非氧化还原反应”)。
(2)某钛铁矿中FeTiO3的含量为76%,该钛铁矿与硫酸反应时Ti转化率为92%,操作I到操作IV的过程中Ti的转化率为96%,则1t该钛铁矿可生产钛白粉 ______ t(所有计算结果保留两位有效数字),能否计算绿矾的产量______?(若能则计算数值,否则说明理由)。
(3)操作I的名称是 ______,操作II包括搅拌、结晶、______,操作II中加入铁粉的目的是______(用离子方程式表示)。
(4)写出操作III中TiOSO4水解的化学方程式: ______ 。
(5)该生产过程中产生的尾气SO2、SO3的处理方法是 ______ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有a、b、c、d四个金属电极,有关的反应装置及部分反应现象如下:
实验装置 | 部分实验现象 |
| a极质量减小,b极质量增加 |
| b极有气体产生,c极无变化 |
| d极溶解,c极有气体产生 |
| 电流计指示在导线中电流从a极流向d极 |
由此可判断这四种金属的活动性顺序是( )
A.a>b>c>dB.b>c>d>aC.d>a>b>cD.a>b>d>c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用甲苯生产邻羟基苯甲酸甲酯: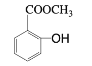 ,下列反应① ~⑥ 是其合成过程,其中某些反应条件及部分反应物或生成物未注明。
,下列反应① ~⑥ 是其合成过程,其中某些反应条件及部分反应物或生成物未注明。
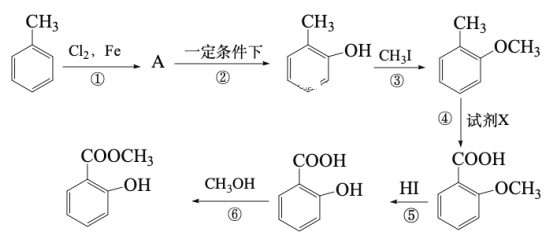
回答下列问题:
(1)有机物A的结构简式为___________________,习惯命名法A的名称为______________。
(2)反应②的化学方程式是________________________________________。
(3)试剂X是___________________。
(4)反应⑥ 的化学方程式是___________________________________。
(5)合成路线中设计③ 、⑤ 两步反应的目的是_____________________________。
(6)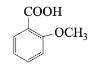 的同分异构体中,既能与NaHCO3发生反应,又能与FeCl3溶液发生显色反应的共有_________种,其中核磁共振氢谱为5组峰,且峰面积比为2:2:2:1:1的有机物结构简式为________________。
的同分异构体中,既能与NaHCO3发生反应,又能与FeCl3溶液发生显色反应的共有_________种,其中核磁共振氢谱为5组峰,且峰面积比为2:2:2:1:1的有机物结构简式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验的推理正确的是
A.向CuSO4·5H2O晶体中滴加浓硫酸,晶体表面变为白色,说明浓硫酸具有强氧化性
B.向溶液X中滴加BaCl2溶液,有白色沉淀生成,说明溶液X中含![]()
C.向品红溶液中通入气体Y,溶液变为无色,加热后变红,说明Y为SO2
D.向溶液Z中通入Cl2,再滴加KSCN溶液后变红,说明溶液Z中含Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现在大量盆栽鲜花都施用了S诱抗素制剂,以保持鲜花盛开。S诱抗素的分子结构如图,下列关于该分子说法正确的是( )

A.该物质的分子式为:C15H18O4
B.1mol该物质可以与2molNa反应,2molNaOH溶液反应
C.1mol该物质可以与4molH2发生加成反应
D.含有碳碳双键、苯环、羟基、羰基
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作、现象和结论均正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 将铜粉加入1.0mol/LFe2(SO4)3溶液中 | 溶液变为蓝色 | 金属铁比铜活泼 |
B | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 熔化后的液态铝不滴落下来 | 氧化铝的熔点高于铝的熔点 |
C | 常温下,用pH计测0.1mol/LNaX溶液和0.1mol/LNa2CO3溶液的pH | 前者小于后者 | 酸性:HX>H2CO3 |
D | 向10%的蔗糖溶液中加入少量稀硫酸,水浴加热一段时间,再加入银氨溶液 | 未出现光亮银镜 | 蔗糖未发生水解 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物M具有广谱抗菌活性,合成M的反应可表示如下:
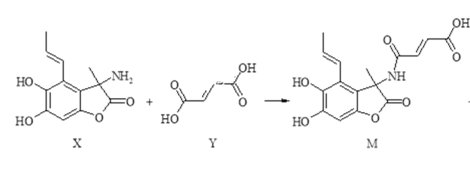 +H2O
+H2O
下列说法正确的是( )
A.X分子中有5种官能团
B.Y分子中所有原子不可能在同一平面内
C.可用FeCl3溶液或NaHCO3溶液鉴别X和M
D.在NaOH溶液中,1molX最多可与4molNaOH发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,容积2L的密闭容器中,将2molL气体和3molM气体混合,发生如下反应:2L(g)+3M(g)![]() xQ(g)+3R(g),10s末,生成2.4molR,测得Q的浓度为0.4mol·L-1。计算:
xQ(g)+3R(g),10s末,生成2.4molR,测得Q的浓度为0.4mol·L-1。计算:
(1)10s末L的物质的量浓度为_________。
(2)前10s内用M表示的化学反应速率为_________。
(3)化学方程式中x值为_________。
(4)L的转化率是_________。
(5)下列还可以说明该反应已达平衡的是_________(填序号)。
①体系内压强不再改变
②容器内气体的密度不再改变
③混合气体的平均相对分子质量不再改变
④v正(M)=2v逆(R)
⑤n(L)∶n(M)∶n(R)=2∶3∶3
(6)在其它条件不变时,减小压强,化学反应反应速率_________(增大、减小、不变)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com