
 在0.2L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,回答下列问题:
在0.2L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,回答下列问题:| n |
| V |
| 0.5mol/L×0.2L |
| 1L |


 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 的系统命名是:
的系统命名是: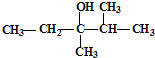 的键线式是
的键线式是 是由一种单体缩聚而成的,该单体的结构简式为
是由一种单体缩聚而成的,该单体的结构简式为查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、含有离子键和共价键的化合物一定是离子化合物 |
| B、所有元素原子的最外层电子数等于该元素的最高化合价 |
| C、元素的相对原子质量数值上等于该元素的原子序数 |
| D、多电子原子中,在离核较近的区域内运动的电子能量较高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、P和S属于第三周期元素,P原子半径比S大 |
| B、Na和Rb属于第ⅠA族元素,Rb失电子能力比Na强 |
| C、C和Si属于第ⅣA族元素,SiH4比CH4稳定 |
| D、Cl和Br属于第ⅦA族元素,HClO4酸性比HBrO4弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 两种气态烃组成的混合气体,完全燃烧后得到CO2和H2O的物质的量与混合烃物质的量的关系如图所示,则下列对混合烃的判断正确的是( )
两种气态烃组成的混合气体,完全燃烧后得到CO2和H2O的物质的量与混合烃物质的量的关系如图所示,则下列对混合烃的判断正确的是( )| A、②⑤⑥ | B、②④⑥ |
| C、②④ | D、②③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com