
【题目】下图是一种正投入生产的大型蓄电系统。放电前,被膜隔开的电解质为Na2S2和NaBr3,放电后分别变为Na2S4和NaBr。下列叙述正确的是

A. 放电时,负极反应为3NaBr-2e-==NaBr3+2Na+
B. 充电时,阳极反应为2Na2S2-2e-== Na2S4+2Na+
C. 放电时,Na+经过离子交换膜,由b池移向a池
D. 用该电池电解饱和食盐水,产生2.24LH2时,b池生成17.40g Na2S4
【答案】C
【解析】放电前,被膜隔开的电解质为Na2S2(右罐)和NaBr3(左罐),则Na2S2在负极失电子,NaBr3在正极得电子;充电时,阴极为负极的逆反应,阳极为正极的逆反应;A.放电时,负极Na2S2失电子,则负极的电极反应式为:2S22--2e-═S42-,故A错误;B.充电时,阳极上Br-失电子转化为Br3-,则阳极的电极反应式为:3Br--2e-=Br3-,故B错误;C.电池放电时,Na2S2和NaBr3反应,则电池的总反应方程式为:2Na2S2+NaBr3=Na2S4+3NaBr,Na+经过离子交换膜,由b池移向a池,故C正确;D. 用该电池电解饱和食盐水,产生2.24LH2时,此气体不是标准状况下的体积,无法进行换算,则b池生成Na2S4的质量不一定是17.40g,故D错误.答案选C。


 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:高中化学 来源: 题型:
【题目】某粗铜产品中含有Zn、Ag、Au等杂质,如图所示,用CH3OH-碱性燃料电池电解硫酸铜溶液。闭合电键K进行电解。下列说法中不正确的是( )
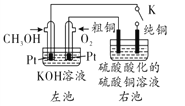
A. 左池负极反应式为CH3OH -6e-+8OH-=CO32-+ 6H2O
B. 通电一段时间后,Ag、Au杂质金属沉积在电解槽底部
C. 若粗铜电极质量减少6.4g,则纯铜电极增重大于6.4g
D. 电解过程中右池纯铜和粗铜分别为阴极和阳极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲同学在实验室用图甲装置制取乙酸乙酯。回答下列问题:

(1)实验中采用小火加热的目的是__________。
(2)加热A—会儿后,发现忘记加碎瓷片,应采取的正确操作是__________。
(3)浓硫酸的作用是__________。
(4)乙同学采用图乙装罝,图中球形干燥管除起冷凝作用外,另一要重用是__________。
(5)若要把制得的乙酸乙酯分离出来,应采用的实验操作是__________。
(6)下列描述能说明乙醇与乙酸的酯化反应己达到化学平衡状态的有(填序号)____。
①单位时间里生成1mol CH3COOCH2CH3的同时生成1 mol H2O
②单位时间里生成1mol CH3COOCH2CH3的同时消耗1mol CH3COOH
③单位时间里消耗1molCH3CH2OH的同时消耗1 mol CH3COOH
④混合物中各物质的浓度不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【选修5——有机化学基础】以芳香族化合物A和有机物D为原料,制备异戊酸薄荷醇酯(M)和高聚物(N)的一种合成路线如下图所示(部分反应条件已省略):

已知: I.A→B的原了利用率为100%;
II. ![]() (R1、R2表示氢原子或烃基)。
(R1、R2表示氢原子或烃基)。
请回答下列问题:
(1)用系统命名法对G命名,其化学名称为______________________。
(2)E的结构简式为____________________________。
(3)A→B的反应类型为_______。B分子中最多有____个原子共平面。
(4)C+G→M的化学方程式为_____________________________________。
(5)同时满足下列条件的B的同分异构体有______种(不考虑立体异构)。
①苯环上连有两个取代基 ②能发生银镜反应
(6)参照上述合成路线和信息,以苯乙烯为原料(无机试剂任选),设计制备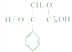 的合成路线______。
的合成路线______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于氨的下列叙述中,不正确的是( )
A.液氨是纯净物
B.实验室制氨气的方法是加热NH4Cl
C.氨易液化,因此可用来作制冷剂
D.氨极易溶于水,因此可用来作喷泉实验
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质的转化关系如图所示(部分物质和条件已略去),A是一种淡黄色粉末,B是某种矿物中的主要成分,D、Y是空气含量最多的两种气体,J是一种紫红色金属,X是最常见的无色液体.
(1)A的化学式为
(2)Y的电子式为
(3)I与J反应的化学方程式为
(4)C与B在溶剂X中反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G七种短周期主族元素,它们的原子序数依次增大。B原子的最外层电子数是其次外层电子数的2倍。A的一种原子中,质量数与质子数之差为零。D元素原子的最外层电子数为m,次外层电子数为n。E元素原子的L层上电子数为(m+n),M层上电子数为![]() 。F与D同主族。请回答下列问题:
。F与D同主族。请回答下列问题:
(1)B元素在周期表中的位置是________。
(2)C与E形成的化合物E3C属于________(填“原子”“离子”或“分子”)晶体。
(3)简单D离子和E离子的半径由大到小____________(填离子符号)
(4)B和D简单气态氢化物的稳定性; _______<_______(填化学式)
(5)F的一种氧化物中氧的质量分数为50%,写出该氧化物与G单质水溶液反应的化学方程式:__________________________________________________。
(6)已知:甲+H2O→丙+丁,该反应不是氧化还原反应。若甲是由N和Cl元素组成的化合物,其分子结构模型如下图所示,丙具有漂白性。则甲中氯元素的化合价是________,丁与H2O有相同的电子总数,则丁的结构式为________。
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国古代炼丹家魏伯阳所著《周易参同契》是世界上现存最早的一部炼丹专著。书中描写到:“金人于猛火,色不夺精光。”这句话是指金在强热条件下( )
A.活泼B.稳定C.易被氧化D.易被还原知识点
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com