
| A. | O-16可以表示为:${\;}_{16}^{32}$O | B. | 对硝基甲苯的结构简式: | ||
| C. | 羟基的电子式: | D. | 二氧化碳分子的比例模型: |
分析 A.元素左上角数字为质量数,左下角数字为质子数,氧元素质子数为8;
B.对硝基甲苯中苯环连接氮原子;
C.氧原子与氢原子通过一对共用电子对连接,羟基中的氧原子含有一个未成对电子;
D.二氧化碳分子中,碳原子半径大于氧原子.
解答 解:A.元素左上角数字为质量数,O-16可以表示为:$\underset{\stackrel{18}{\;}}{8}\underset{\stackrel{\;}{O}}{\;}$,故A错误;
B.对硝基甲苯中,硝基的N原子与苯环相连,正确的结构简式为 ,故B错误;
,故B错误;
C.羟基结构简式为-0H,电子式为 ,故C正确;
,故C正确;
D.二氧化碳分子中碳原子半径大于氧原子,二氧化碳正确的比例模型为: ,故D错误;
,故D错误;
故选C.
点评 本题考查了常见化学用语的判断,题目难度不大,注意掌握电子式、结构简式等的概念及正确表示方法,试题有利于培养学生规范答题的能力.


科目:高中化学 来源: 题型:解答题
 ,Z在周期表中的位置为第三周期ⅢA族.
,Z在周期表中的位置为第三周期ⅢA族. ,XY2的电子式为
,XY2的电子式为 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题

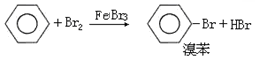 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将78g Na2O2与过量CO2反应转移的电子数为2NA | |
| B. | 1molN2与4mol H2反应生成的NH3分子数为2NA | |
| C. | 标准状况下,2.24LCCl4中所含原子数为0.5NA | |
| D. | 标准状况下,18gD2O中所含电子数为9NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
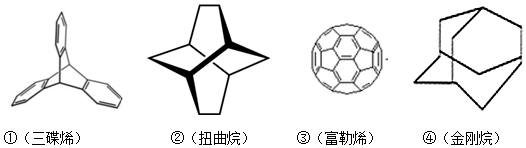
| A. | ①③均能发生加成反应 | B. | ①④互为同分异构体 | ||
| C. | ①②③④均属于烃 | D. | ①②③④的一氯代物均只有一种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向新制的氯水中加入NaHCO3粉末,有气泡产生,说明氯元素的非金属性强于碳 | |
| B. | 向Fe(NO3)3溶液中通入适量SO2气体后,再滴加BaCl2溶液,产生白色沉淀,说明Fe3+能够将H2SO3氧化为H2SO4 | |
| C. | 向NaOH溶液中滴加少量的MgCl2溶液,产生白色沉淀,然后再滴加足量的CuCl2溶液,沉淀变蓝色,说明 Ksp[Cu(OH)2]<Ksp[Mg(OH)2] | |
| D. | 用铂丝蘸取少量某溶液进行焰色反应,火焰呈紫色,说明该溶液一定含有钾元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 太阳能热水器,太阳能电池、由玉米制乙醉部涉及生物质能的利用 | |
| B. | “地沟油”禁止食用,但经加工处理后可用来制造肥皂和生物柴油 | |
| C. | 以淀粉浓液作指示剂,用已知浓度的碘溶液来测定食品中SO2的残留量 | |
| D. | 雾霾属于分散系,减少生产生活中产生的扬尘可以减少雾霾天气的形成 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu(OH)2+HCl;Cu(OH)2+CH3COOH | B. | Na2CO3+H2SO4;Na2CO3+HCl | ||
| C. | CaCO3+H2SO4;CaCO3+HCl | D. | BaCl2+H2SO4;Ba(OH)2+H2SO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com