
分析 纯水存在电离平衡,电离出的氢离子浓度和氢氧根离子浓度相同,据此得出该纯水中氢氧根离子浓度;温度不变,水的离子积不变,计算出该温度下水的离子积,然后根据水的离子积表达式计算出滴入盐酸后溶液中的氢氧根离子浓度.
解答 解:某温度下纯水中的c(H+)=2×10-7mol/L,则此时溶液中的c(OH-)=c(H+)=2×10-7mol/L;
若温度不变,滴入稀盐酸,使c(H+)=4×10-3mol/L,溶液中则溶液中c(H+)•c(OH-)=2×10-7×2×10-7=4×10-14,
温度不变,则水的离子积不变,故c(OH-)=$\frac{4×1{0}^{-14}}{4×1{0}^{-3}}$mol/L=10-11mol/L,
故答案为:2×10-7;10-11.
点评 本题考查了物质的量浓度的计算、水的离子积的计算,题目难度中等,明确水的电离及其影响为解答关键,注意掌握水的离子积及其计算方法,明确物质的量浓度的概念及表达式.


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源: 题型:解答题
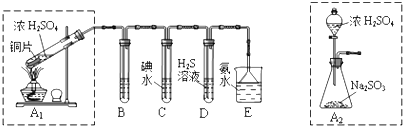
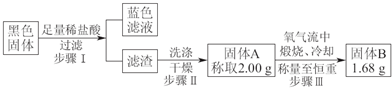
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电负性:X<Y | |
| B. | 周期表中,X可能在Y的右边 | |
| C. | 若X与Y形成化合物,则X显正价,Y显负价 | |
| D. | 气态氢化物的稳定性:HmY强于HnX |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 原子半径:A<B | |
| B. | 原子序数:A<B | |
| C. | 元素所在的周期数:A>B | |
| D. | A的最高正价与B的最低负价的绝对值一定相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | KO2 | B. | K2O2 | C. | K2O3 | D. | K2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| Na2O | Na | AlF3 | AlCl3 | Al2O3 | BCl3 | CO2 | SiO2 |
| 920℃ | 97.8℃ | 1 291℃ | 190℃ | 2 073℃ | -107℃ | -57℃ | 1 723℃ |
| A. | 只要含有金属阳离子的晶体就一定是离子晶体 | |
| B. | 在共价化合物分子中各原子都形成8电子结构 | |
| C. | 金属晶体的熔点不一定比分子晶体的高 | |
| D. | 同族元素的氧化物不可能形成不同类型的晶体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com