
纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的四种方法:
| 方法a | 用炭粉在高温条件下还原CuO |
| 方法b | 用葡萄糖还原新制的Cu(OH)2制备Cu2O; |
| 方法c | 电解法,反应为2Cu + H2O |
| 方法d | 用肼(N2H4)还原新制的Cu(OH)2 |
(1)已知:2Cu(s)+1/2O2(g)=Cu2O(s);△H = -169kJ·mol-1
C(s)+1/2O2(g)=CO(g);△H = -110.5kJ·mol-1
 Cu(s)+1/2O2(g)=CuO(s);△H = -157kJ·mol-1
Cu(s)+1/2O2(g)=CuO(s);△H = -157kJ·mol-1
则方法a发生的热化学方程式是: __ ▲ ___
(2)方法c采用离子交换膜控制电解液中OH-的浓度而制备纳米 Cu2O,装置如右图所示:该电池的阳极反应式为 __ ▲ ___
钛极附近的pH值 __ ▲ ___ (增大、减小、不变)
(3)方法d为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2。该制法的化学方程式为 ▲ ___
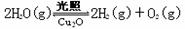 (4)在相同的密闭容器中,用以上方法制得的三种Cu2O分别进行催化分解水的实验: △H>0。水蒸气的浓度随时间t变化如下表所示。
(4)在相同的密闭容器中,用以上方法制得的三种Cu2O分别进行催化分解水的实验: △H>0。水蒸气的浓度随时间t变化如下表所示。
| 序号 |
| 0 | 10 | 20 | 30 | 40 | 50 |
| ① | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
| ② | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
| ③ | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
下列叙述正确的是 __ ▲ ___ (填字母)。
A.实验的温度:T2<T1 B.实验②比实验①所用的催化剂催化效率高
C.实验①前20 min的平均反应速率 v(H2)=7×10-5 mol·L-1 min-1
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:
在一体积为10 L的容器中,通过一定量的CO和H2O,850 ℃时发生反应:
CO(g)+H2O(g)CO2(g)+H2(g)

(1)CO和H2O浓度变化如图,则0~4 min的平均反应速率v(CO)=________mol·L-1·min-1。
(2)如图中4~5 min之间该反应________(填“是”或“否”)处于平衡状态,判断理由_______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
设定下图所示装置中的反应是完全进行的。
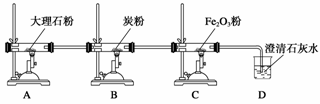
(1)分别写出A、B、C装置中的化学反应方程式:
________________________________________________________________________
________________________________________________________________________;
(2)若D装置中的澄清石灰水是少量的,将可能观察到的现象:________________
________________________________________________________________________;
用化学方程式解释上述现象:_____________________________________________
________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子在指定溶液中一定能大量共存的是
A.使甲基橙变红色的溶液:Mg2+、K+、SO42-、NO3-
B.PH=13的溶液:Na+、Cu2+、HCO3-、NO3--
C.水电离出的c(H+)=10—12mol/L的溶液:K+、Na+、CO32-、Br-
D.0.1mol/L的AgNO3的溶液:H+、K+、SO42-、I-
查看答案和解析>>
科目:高中化学 来源: 题型:
对室温下等pH、等体积的醋酸和盐酸两种溶液分别采取下列措施,有关叙述正确的是
A.加适量的醋酸钠晶体后,两溶液的pH均增大
B.加入足量的苏打固体充分反应后,两溶液中产生的CO2一样多
C.加水稀释2倍后,两溶液的pH均减小
D.加足量的锌充分反应后,盐酸中产生的氢气速率快
查看答案和解析>>
科目:高中化学 来源: 题型:
卫生部发出公告,自2011年5月1日起,禁止在面粉生产中添加过氧化钙(CaO2)等食品添加剂。下列对过氧化钙的叙述错误的是
A.CaO2具有氧化性,对面粉可能具有增白作用
B.CaO2和水反应时,每产生1 mol O2转移电子2 mol
C.CaO2中阴阳离子的个数比为2∶1
D.CaO2和CO2反应的化学方程式为:2CaO2+2CO2 =2Ca CO3+O2
查看答案和解析>>
科目:高中化学 来源: 题型:
在含有Fe3+、Fe2+、Al3+、NH4+的溶液中,加入足量Na2O2固体,微热充分反应后,再加入过量的稀盐酸,完全反应后,离子数目没有变化的是
A.Fe3+ B.Al3+ C.NH4+ D.Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
工业催化剂K3[Fe(C2O4)3]·3H2O是翠绿色晶体,在421~553℃时,分解为Fe2O3、K2CO3、CO、CO2、H2O。实验室由草酸亚铁晶体(FeC2O4·2H2O)、草酸钾(K2C2O4)、草酸(H2C2O4)和双氧水(H2O2)混合制备:
2FeC2O4·2H2O + H2O2+ 3K2C2O4+ H2C2O4=2K3[Fe(C2O4)3]·3H2O
(1)[Fe(C2O4)3]3-的名称是_______________。
(2)制备过程要防止草酸被H2O2氧化,写出草酸被H2O2氧化的化学方程式__________。
(3)配合物的稳定性可以用稳定常数K来衡量,如Cu2+ + 4NH3 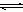 [Cu(NH3)4]2+,其稳定常数表达式为:
[Cu(NH3)4]2+,其稳定常数表达式为: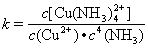 。已知K [Fe(C2O4)3]3-=1020,K [Fe(SCN)3]= 2×103,能否用KSCN溶液检验K3[Fe(C2O4)3]·3H2O中的铁元素? (填“是”、“否”)。 若选“否”,请设计检验K3[Fe(C2O4)3]·3H2O中铁元素的方案。__________________________。
。已知K [Fe(C2O4)3]3-=1020,K [Fe(SCN)3]= 2×103,能否用KSCN溶液检验K3[Fe(C2O4)3]·3H2O中的铁元素? (填“是”、“否”)。 若选“否”,请设计检验K3[Fe(C2O4)3]·3H2O中铁元素的方案。__________________________。
(4)铁元素可形成多种配合物,其中一种配合物钾盐A是有争议的食品添加剂。经组成分析A仅含K、Fe、C、N四种元素。取36.8g A加热至400℃,分解成KCN、Fe3C、C、N2,生成的氮气折合成标准状况下的体积为2.24L,Fe3C质量是C质量的3倍,Fe3C物质的量是氮气物质的量的1/3。则A的化学式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列水解的离子方程式正确的是( )
A.NH4++H2O NH3·H2O+H+ B.Br-+H2O
NH3·H2O+H+ B.Br-+H2O HBr+OH-
HBr+OH-
C.CO32-+2H2O H2CO3+2OH- D.Fe3++3H2O
H2CO3+2OH- D.Fe3++3H2O Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com