
(12分)如下图,通电5 min后,电极5质量增加2.16 g,回答:
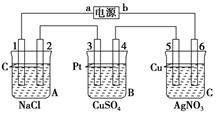
(1)电源:a是________极,b是________极;A池电极反应,电极1:__________;
电极2:____________________________________________________________。
C池电极反应,电极5:________________________________________________;
电极6:______________________________________________________________。
(2)如果B池中共收集到224 mL气体(标准状况),且溶液体积为200 mL(设电解过程中溶液体积不变),则通电前溶液中Cu2+的物质的量浓度为________。
(1)负 正 2H++2e-===H2↑ 2Cl--2e-===Cl2↑ 2Ag++2e-===2Ag Cu-2e-===Cu2+
(2)0.025 mol/L
【解析】
试题分析:(1)通电5 min后,电极5质量增加2.16 g,这说明电极5是阴极,所以电极是阳极。则b是电源的正极,a是电源的负极。因此电极1是阴极,氢离子放电生成氢气,电极反应式是2H++2e-===H2↑。电极2是阳极,溶液中的氯离子放电生成氯气,电极反应式是2Cl--2e-===Cl2↑。C装置中电极5是阴极,溶液中的银离子放电,电极反应式是2Ag++2e-===2Ag。电极6是阳极,但电极是铜电极,所以铜失去电子,电极反应式是Cu-2e-===Cu2+。
(2)电极5生成银的质量是2.16g,物质的量是0.02mol,转移0.02mol电子。B池中共收集到224 mL气体(标准状况),则气体的物质的量是0.01mol。如果气体全部是氧气,则转移电子是0.04mol。显然电子的得失不守恒,所以生成的气体中还含有氢气。根据电子的得失守恒可知,阳极生成氧气的物质的量是0.02mol÷4=0.005mol,所以阴极生成的氢气是0.01mol-0.005mol=0.005mol。则阴极析出的铜的物质的量是(0.02mol-0.005mol×2)÷2=0.005mol,因此电解硫酸铜溶液的物质的量浓度是0.005mol÷0.2L=0.025 mol/L。
考点:考查电极名称的判断、电极反应式的书写以及电解的有关计算
点评:该题的难点在(2)问,需要利用电子守恒,通过讨论得出阴极还有氢气生成,最后再通过电子的守恒计算即可,属于中等难度的试题。


科目:高中化学 来源: 题型:
(12分)如下图,通电5 min后,电极5质量增加2.16 g ,回答:
(1) 电源:a是________极;A池中电极 上产生气体能使湿润KI淀粉试纸变蓝;B池中电极 上发生氧化反应,电解过程中pH (填增大、减小或不变)。
电池电极反应,电极1: ;电极4: 。
A池电池总反应 。
C池电池总反应 。
(2) 如果B池中共收集到224 mL气体(标准状况) ,且溶液体积为200mL(设电解过程中溶液体积不变),则通电前溶液中Cu2+的物质的量浓度为 。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年内蒙古巴市中学高二12月月考化学试卷(带解析) 题型:填空题
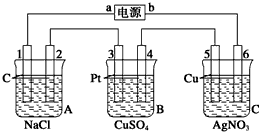
(12分)如下图,通电5 min后,电极5质量增加2.16 g,回答:
(1)电源:a是________极,b是________极;A池电极反应,电极1:__________;
电极2:____________________________________________________________。
C池电极反应,电极5:________________________________________________;
电极6:______________________________________________________________。
(2)如果B池中共收集到224 mL气体(标准状况),且溶液体积为200 mL(设电解过程中溶液体积不变),则通电前溶液中Cu2+的物质的量浓度为________。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年四川省高三上学期8月月考化学试卷 题型:实验题
(12分)如下图,通电5 min后,电极5质量增加2.16 g ,回答:

(1) 电源:a是________极 ;A池中电极 上产生气体能使湿润KI淀粉试纸变蓝;B池中电极 上发生氧化反应,电解过程中pH (填增大、减小或不变)。
电池电极反应,电极1: ;电极4: 。
A池电池总反应 。
C池电池总反应 。
(2) 如果B池中共收集到224 mL气体(标准状况) ,且溶液体积为200 mL(设电解过程中溶液体积不变),则通电前溶液中Cu2+的物质的量浓度为 。
查看答案和解析>>
科目:高中化学 来源:专项题 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com