
【题目】某燃料电池如图所示,两电极A、B材料都是石墨,下列说法不正确的是

A. 氧气在正极发生还原反应
B. 若电解质为氢氧化钠溶液,则负极反应式为 H2-2e-+2OH-=2H2O
C. 电子由电极a流经电解液到电极b
D. 若正极消耗的气体质量为4 g,则转移的电子的物质的量为0.5 mol
【答案】C
【解析】氢氧燃料碱性电池中,负极上通入燃料,燃料失电子和氢氧根离子反应生成水,正极上通入氧气,氧气得电子和水反应生成氢氧根离子,据此分析解答。
A.b电极上氧气得电子发生还原反应作电池的正极,选项A正确;B. 若电解质为氢氧化钠溶液,则负极上氢气失电子产生的氢离子与氢氧根离子结合生成水,电极反应式为:H2-2e-+2OH-=2H2O,选项B正确;C、根据以上分析,原电池中电子从负极流向正极,即从a电极流出经导线流向b电极,选项C不正确;D.正极发生还原反应,电极方程式为O2+2H2O+4e-=4OH-,若正极消耗的气体质量为4克,即0.125mol,则转移的电子的物质的量为0.125mol×4=0.5mol,选项D正确。答案选C。


科目:高中化学 来源: 题型:
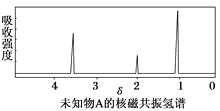
【题目】已知某有机物A的红外光谱和核磁共振氢谱如图所示,下列说法不正确的是

A. 由红外光谱可知,该有机物中至少有三种不同的化学键
B. 由核磁共振氢谱可知,该有机物分子中有三种不同的氢原子
C. 仅由核磁共振氢谱无法得知其分子中的氢原子总数
D. 若A的化学式为C2H6O,则其结构简式为CH3—O—CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组的同学为探究原电池原理,设计如图所示装置,将锌、铜通过导线相连,置于稀硫酸中。

(1)外电路,电子从__________极流出。溶液中,阳离子向_______极移动。
(2)若反应过程中有0.2 mol电子发生转移,则生成的气体在标准状况下的体积为______________。
(3)该小组同学将稀硫酸分别换成下列试剂,电流计仍会偏转的是_____(填序号)。
A.无水乙醇 B.醋酸溶液 C.CuSO4溶液 D.苯
(4)实验后同学们经过充分讨论,认为符合某些要求的化学反应都可以通过原电池来实现。下列反应可以设计成原电池的是____________(填字母代号)。
A. NaOH+HCl=NaCl+H2O B. 2H2+O2=2H2O
C. Fe+2FeCl3=3FeCl2 D. 2H2O=2H2↑+2O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】具有抗菌作用的白头翁素衍生物M的合成路线如下图所示:

已知:ⅰ.RCH2Br![]() R—HC=CH—R'
R—HC=CH—R'
ⅱ.R—HC=CH—R'![]()
![]()
ⅲ.R—HC=CH—R'![]()
![]() (以上R、R'、R″代表氢、烷基或芳基等)
(以上R、R'、R″代表氢、烷基或芳基等)
(1)D中官能团名称为_____,A的化学名称为_____。
(2)F的结构简式为_____,则与F具有相同官能团的同分异构体共_____种(考虑顺反异构,不包含F)。
(3)由G生成H的化学方程式为_____,反应类型为_____。
(4)下列说法不正确的是_____(选填字母序号)。
a.可用硝酸银溶液鉴别B、C两种物质
b.由H生成M的反应是加成反应
c.1 mol E最多可以与4 mol H2发生加成反应
d.1 mol M与足量NaOH溶液反应,消耗4 mol NaOH
(5)以乙烯为起始原料,结合已知信息选用必要的无机试剂,写出合成![]() 的路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。__________
的路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于胶体和溶液的说法中,正确的是( )
A.胶体粒子的直径大于100nm
B.用过滤的方法可以分离胶体和溶液
C.光线通过时,胶体产生丁达尔效应,溶液则无丁达尔效应
D.将饱和氯化铁溶液滴入稀氢氧化钠溶液中加热,可得氢氧化铁胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,下列溶液的离子浓度关系式正确的是( )
A. pH=5的H2S溶液中,c(H+)=c(HS-)=1×10-5mol·L-1
B. pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1
C. pH=2的乙二酸(H2C2O4)溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+c(H+)=c(OH-)+c(HC2O4-)
D. pH相同的①CH3COONa②NaHCO3③NaClO三种溶液的c(Na+):①>②>③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色透明溶液,在酸性环境下能大量共存的离子组是( )
A.Na+、SO42-、CO32-、Cl-
B.Mg2+、Cl-、Na+、NO3-
C.K+、MnO4-、NO3-、Fe2+
D.Cu2+、Cl-、H+、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的定容容器中,发生反应:2A(g)+B(s)![]() C(g)+D(g),下列描述中能表明反应已达到平衡状态的是
C(g)+D(g),下列描述中能表明反应已达到平衡状态的是
①混合气体的压强不变
②混合气体的密度不变
③C(g)的物质的量浓度不变
④容器内A、C、D三种气体的浓度之比为2:1:1
⑤单位时间内生成n molD,同时生成2n mol A
⑥单位时间内生成n molC,同时消耗n mol D
A. ①②③ B. ③④⑥ C. ②③⑤⑥ D. 只有 ③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,常温下是一种橙黄色有恶臭的液体,它的分子结构与H2O2类似,遇水易水解,产生能使品红褪色的气体。S2Cl2可由干燥氯气通入熔融的硫中制得。
(1) 写出二氯化二硫(S2Cl2)的电子式___________
(2) 写出二氯化二硫(S2Cl2)遇水反应的化学方程式____________。
II.锌元素与人的智力有密切关系,如ZnSO4·7H2O、ZnO等均具有药物价值。
(1)工业上制备ZnSO4·7H2O的方法很多,可由粗ZnO(含Fe2+、Mn2+、Cd2+、Ni2+)通过以下流程完成:

① 试写出加入稀高锰酸钾溶液时的离子方程式:_________、__________。
② 流程③中的金属可以用(____)
A.Na B.Al C.Zn D.Cu
③ 流程④中调pH=1目的为___________________。
(2) 氧化锌的制备:取精制的硫酸锌溶液慢慢加入碳酸钠溶液,边加边搅拌使气体完全逸出,并使pH约为6.8左右,煮沸至沉淀析出,倾去上层清液,用热水洗涤到无SO42-为止,过滤干燥后得固体ZnCO3·2Zn(OH)2·2H2O转至仪器A中,煅烧至完全分解,冷却得固体ZnO。
① 仪器A名称为______。
② 写出硫酸锌溶液中慢慢加入碳酸钠溶液时的化学方程式________。
③ 如何证明固体A已煅烧至完全分解?_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com