
根据环保要求,在处理有氰电镀废水时,剧毒的CN-离子在催化剂TiO2颗粒作用下,
先用NaClO将CN-离子氧化成CNO-(CN-和CNO-中N元素均为-3价),再在酸性条件下继续与NaClO反应生成N2、CO2和Cl2。环保工作人员在密闭系统中用下图装置进行实验,测定
CN-被处理的百分率。
现将浓缩后含CN-离子的污水与过量NaClO溶液的混合液共200 mL(其中CN-的浓度为0.2 mol/L)倒入甲中,塞上橡皮塞,一段时间后,打开橡皮塞和活塞,使溶液全部放入乙中,关闭活塞。回答下列问题:
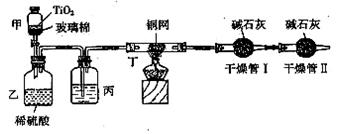
(1)根据题意,写出相关主要反应的离子方程式:
甲中的反应:
乙中的反应:
(2)上述实验是通过测定CO2的量来确定对CN-的处理效果。
丙装置中的试剂是 ,丁装置的目的是 ;干燥管Ⅱ的作用是 。
(3)假定上述每一个装置都充分吸收,则利用该装置测得的CN-被处理的百分率与实际值相比
__________(填“偏高”或“偏低”),简述可能的原因: 。
(4)若干燥管Ⅰ中碱石灰增重1.408 g,则该实验中测得CN-被处理的百分率为 。
科目:高中化学 来源: 题型:
熔融盐燃料电池具有高的发电效率,因而受到重视。用Li2CO3和Na2CO3的熔融盐混合物作电解质,一极通CO气体,另一极通O2和CO2混合气体,可制得在650℃下工作的燃料电池。已知该电池总反应为:2CO+O2=2CO2。则下列说法中正确的是( )
A.通CO的一极是电池的正极,
B.该电池工作过程中需不断补充CO和O2,CO2可循环利用
C.负极反应式:O2+2CO2+4e-==2CO32-
D.该电池工作过程中有蓝色火焰产生
查看答案和解析>>
科目:高中化学 来源: 题型:
已知某有机物A:
①由C、H、O三种元素组成,经燃烧分析实验测定其碳的质量分数是64.86%,氢的质量分数是13.51% ②下图是该有机物的质谱图,
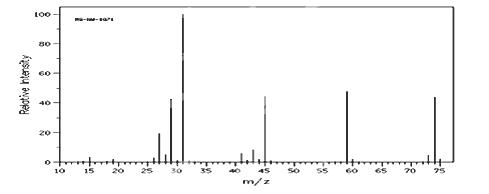
③A的红外光谱图上有C-H键、O-H键、C-O键的振动吸收峰。
④A的核磁共振氢谱有两个峰。请回答:
(1)A的实验式(最简式)为 ,分子式为 。
若无以上质谱图,能否确定分子式 。
(2)A的结构简式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
利用下列实验装置进行的相应实验,不能达到实验目的的是

A.用图1所示装置可制取氨气
B.用图2所示装置可分离CH3CH2OH和CH3COOC2H5混合液
C.用图3所示装置可制取乙烯并验证其易被氧化
D.用图4所示装置可说明浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
自瑞士ETH天文研究所的Ansgar Grimberg等的研究结果表明,太阳气体中存在大量的20Ne和22Ne。下列关于20Ne和22Ne的说法正确的是
A.20Ne和22Ne互为同位素 B.20Ne和22Ne是同一种核素
C.20Ne的原子核中有20个质子 D.22Ne的原子核中有22个中子
查看答案和解析>>
科目:高中化学 来源: 题型:
几种短周期元素的原子半径及主要化合价如下表
| 元素代号 | L | M | X | R | T |
| 原子半径(nm) | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
下列说法正确的是
A. L、T形成的简单离子核外电子数相等 B.R的氧化物对应的水化物呈强碱性
C.X单质在氧气中燃烧生成XO3 D.离子半径大小:r(M3+)> r(T2-)
查看答案和解析>>
科目:高中化学 来源: 题型:
推进器中盛有强还原剂肼(N2H4)和强氧化剂液态双氧水。当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热。已知0.4mol液态肼与足量液态双氧水反应,生成氮气和水蒸气,放出256.652KJ的热量。
(1)写出过氧化氢的电子式___________________。
(2)该反应的热化学方程式为_________________________________________________。
1mol肼完全反应转移电子数 。
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是 。
(4)又已知H2O(l)==H2O(g);△H = +44kJ∙mol-1,由16g液态肼与液态双氧水反应生成液态水时放出的热量是 kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室可提供下列实验操作:①滴加AgNO3溶液;②加NaOH溶液;③加热;④加催化剂MnO2;⑤加蒸馏水过滤后取滤液;⑥过滤后取滤渣;⑦用HNO3酸化。如要鉴定 1-氯丙烷中的氯元素,从中选择合适的操作步骤是
1-氯丙烷中的氯元素,从中选择合适的操作步骤是
A.③⑤⑦① B.②③⑦① C.②⑤⑦① D.④②⑥①
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com