
| A. | 过程中可能有:c(Na+)>c(OH-)=c(CH3COO-)>c(H+) | |
| B. | 整个过程中都有:c(OH-)-c(H+)=c(Na+)-c(CH3COO-) | |
| C. | 当滴入10.0 mLNaOH溶液时有:c(CH3COOH)-c(CH3COO-)═2[c(OH-)-c(H+)] | |
| D. | 当滴入10.0 mLNaOH溶液时混合溶液的pH=4.75,则:c(CH3COO-)>c(CH3COOH)>c(Na+)>c(H+)>c(OH-) |
分析 25℃时,向10.0mL 0.2mol•L-1CH3COOH溶液中逐滴滴入0.1mol•L-1的NaOH溶液,滴加NaOH溶液过程中溶质依次为CH3COOH→CH3COOH和CH3COONa→CH3COONa→CH3COONa、NaOH,
A.当溶液中溶质为CH3COONa、NaOH,溶液呈碱性,可能存在c(OH-)=c(CH3COO-);
B.任何电解质溶液中都存在电荷守恒,根据电荷守恒判断;
C.当滴入10.0 mLNaOH溶液时,溶液中溶质为等物质的量浓度的CH3COOH和CH3COONa,根据电荷守恒和物料守恒判断;
D.当滴入10.0 mLNaOH溶液时混合溶液的pH=4.75,溶液中溶质为等物质的量浓度的CH3COOH和CH3COONa,溶液呈酸性,说明CH3COOH电离程度小于CH3COONa水解程度.
解答 解:25℃时,向10.0mL 0.2mol•L-1CH3COOH溶液中逐滴滴入0.1mol•L-1的NaOH溶液,滴加NaOH溶液过程中溶质依次为CH3COOH→CH3COOH和CH3COONa→CH3COONa→CH3COONa、NaOH,
A.当溶液中溶质为CH3COONa、NaOH,溶液呈碱性,可能存在c(OH-)=c(CH3COO-),结合物料守恒知,溶液中离子浓度为c(Na+)>c(OH-)=c(CH3COO-)>c(H+),故A正确;
B.任何电解质溶液中都存在电荷守恒,根据电荷守恒得c(H+)+c(Na+)=c(OH-)+c(CH3COO-),所以得c(OH-)-c(H+)=c(Na+)-c(CH3COO-),故B正确;
C.当滴入10.0 mLNaOH溶液时,溶液中溶质为等物质的量浓度的CH3COOH和CH3COONa,根据电荷守恒得c(H+)+c(Na+)=c(OH-)+c(CH3COO-),根据物料守恒得2c(Na+)=c(CH3COOH)+c(CH3COO-),所以得c(CH3COOH)-c(CH3COO-)═2[c(OH-)-c(H+)],故C正确;
D.当滴入10.0 mLNaOH溶液时混合溶液的pH=4.75,溶液中溶质为等物质的量浓度的CH3COOH和CH3COONa,溶液呈酸性,说明CH3COOH电离程度小于CH3COONa水解程度,结合物料守恒得c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+)>c(OH-),故D错误;
故选D.
点评 本题考查酸碱混合溶液定性判断,为高频考点,明确溶液中溶质及其性质、电解质溶液酸碱性是解本题关键,注意电荷守恒、物料守恒的应用,易错选项是D.


科目:高中化学 来源: 题型:选择题
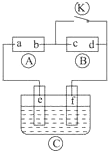 如图
如图  为直流电源,
为直流电源, 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸, 为电镀槽,接通电路后发现
为电镀槽,接通电路后发现 上的c点显红色,为实现铁上镀锌,接通
上的c点显红色,为实现铁上镀锌,接通 后,使c、d两点短路.下列叙述正确的是 ( )
后,使c、d两点短路.下列叙述正确的是 ( )| A. | a为直流电源的负极 | B. | c极发生的反应为2H++2e═-H2↑ | ||
| C. | f电极为锌板 | D. | e极发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 13C与14C属于同一种元素,它们互为同位素 | |
| B. | 28g乙烯和氮气的混合气体中含有NA个气体分子 | |
| C. | 海轮外壳上镶入锌块,可减缓船体的腐蚀 | |
| D. | 常温下,1mol•L-1的 Na2CO3溶液中阴离子总数大于2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

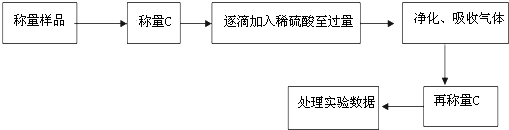
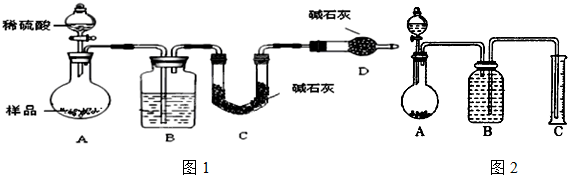
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
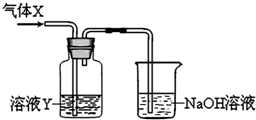
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | CH3COOH溶液中离子浓度的关系满足:c(H+)>c(CH3COO-) | |
| B. | CH3COOH溶液中加入少量CH3COONa固体,平衡逆向移动 | |
| C. | 0.1mol/L的CH3COOH溶液加水稀释,溶液中的离子浓度均减小 | |
| D. | 常温下,pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合后,溶液的pH=7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ag | B. | Zn(OH)2 | C. | Ag2O | D. | Zn |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
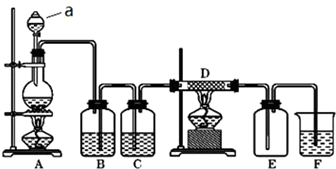

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com