
某固体物质X在一定条件下分解:2X=Y+2Z+4W,产物均为气体,现测得生成的混和气体对氧气的相对密度为0.714,则X的相对分子质量约为
| A.22.85 | B.79.97 | C.159.94 | D.45.69 |
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
①向试管中滴加液体时,为不使液体滴到试管外应将胶头滴管伸入试管中;
②用一团脱脂棉包裹适量的Na2O2,滴入几滴水后脱脂棉燃烧;
③在某未知溶液中滴加几滴BaCl2溶液,产生白色沉淀,再滴入足量的稀盐酸,沉淀不消失,说明原未知溶液中含有![]() ;
;
④酸碱中和滴定过程中,眼睛始终要注视着滴定管中溶液的体积变化,以防滴定过头;
⑤配制100 mL 1.00 mol·L-1 NaCl溶液时,用托盘天平称取
⑥将SO2通入紫色石蕊试液,紫色石蕊试液先变红后变无色;
⑦将NaOH溶液滴入AlCl3溶液中和将AlCl3溶液滴入NaOH溶液中,现象相同;
⑧在一定量的浓硝酸中加入足量的铜,产生气体的速率越来越小,气体的颜色越来越浅;
⑨将一束亮光分别通过红褐色氢氧化铁胶体和无色的硅酸胶体,前者可以看到一条光亮的通路,后者则看不到;
⑩在盛有某物质X溶液的试管中滴加适量的银氨溶液,水浴加热产生银镜,则X一定是醛。
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
已知2A(g)+B(g) ![]() 2C(g),△H=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2molA和1molB,在500℃时充分反应达平衡后C的浓度为ωmol/L,放出热量为b kJ。
2C(g),△H=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2molA和1molB,在500℃时充分反应达平衡后C的浓度为ωmol/L,放出热量为b kJ。
⑴比较a b(填“>”“=”或“<”)。
⑵下表为不同温度下该反应的平衡常数。由此可推知,表中T1 T2(填“>” “=”或“<”)。
| T/K | T1 | T2 | T3 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
若在原来的容器中,只加入2molC,500℃时充分反应达平衡后,吸收热量为c kJ,C 的浓度 (填“>”、“=”或“<”)ωmol/L,a、b、c之间满足何种关系 (用代数式表示)。
⑶在相同条件下要想得到2a kJ热量,加入各物质的物质的量可能是 。
A.4molA和2molB B.4molA、2molB和2molC
C.4molA和4molB D.6molA和4molB
⑷为使该反应的反应速率增大,且平衡向正反应方向移动的是 。
A.及时分离出C气体 B.适当升高温度
C.增大B的浓度 D.选择高效催化剂
⑸若将上述容器改为恒压容器(反应前体积相同),起始时加入2molA和1molB,500℃时充分反应达平衡后,放出热量为d kJ,则d b(填“>”“=”或“<”),理由是 。
⑹在一定温度下,向一个容积可变的容器中,通入3molA和2molB及固体催化剂,使之反应,平衡时容器内气体压强为起始时的90%。保持同一反应温度,在相同容器中,将起始物质的量改为4molA、3molB和2molC,则平衡时A的百分含量 (填“不变”“变大”“变小”或“无法确定”)。
⑺某温度时,卤化银(AgX,X=Cl,Br,I)的3条溶解平衡曲线如图所示,AgCl,AgBr,AgI的Ksp依次减小。已知pAg=-lgc(Ag+),pX=-lgc(X-),利用pX-pAg的坐标系可表示出 AgX的溶度积与溶液中的c(Ag+)和c(X-)的相互关系。下列说法错误的是
A.A线是AgCl,C线是AgI
B.e点表示由过量的KI与AgNO3反应产生AgI沉淀
C.d点是在水中加入足量的AgBr形成的饱和溶液
D.B线一定是AgBr
查看答案和解析>>
科目:高中化学 来源:2010-2011学年浙江省高三高考全真压轴考试(理综)化学试题 题型:填空题
已知2A(g)+B(g)  2C(g),△H=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2molA和1molB,在500℃时充分反应达平衡后C的浓度为ωmol/L,放出热量为b kJ。
2C(g),△H=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2molA和1molB,在500℃时充分反应达平衡后C的浓度为ωmol/L,放出热量为b kJ。
⑴比较a b(填“>”“=”或“<”)。
⑵下表为不同温度下该反应的平衡常数。由此可推知,表中T1 T2(填“>” “=”或“<”)。
|
T/K |
T1 |
T2 |
T3 |
|
K |
1.00×107 |
2.45×105 |
1.88×103 |
若在原来的容器中,只加入2molC,500℃时充分反应达平衡后,吸收热量为c kJ,C 的浓度 (填“>”、“=”或“<”)ωmol/L,a、b、c之间满足何种关系 (用代数式表示)。
⑶在相同条件下要想得到2a kJ热量,加入各物质的物质的量可能是 。
A.4molA和2molB B.4molA、2molB和2molC
C.4molA和4molB D.6molA和4molB
⑷为使该反应的反应速率增大,且平衡向正反应方向移动的是 。
A.及时分离出C气体 B.适当升高温度
C.增大B的浓度 D.选择高效催化剂
⑸若将上述容器改为恒压容器(反应前体积相同),起始时加入2molA和1molB,500℃时充分反应达平衡后,放出热量为d kJ,则d b(填“>”“=”或“<”),理由是 。
⑹在一定温度下,向一个容积可变的容器中,通入3molA和2molB及固体催化剂,使之反应,平衡时容器内气体压强为起始时的90%。保持同一反应温度,在相同容器中,将起始物质的量改为4molA、3molB和2molC,则平衡时A的百分含量 (填“不变”“变大”“变小”或“无法确定”)。
⑺某温度时,卤化银(AgX,X=Cl,Br,I)的3条溶解平衡曲线如图所示,AgCl,AgBr,AgI的Ksp依次减小。已知pAg=-lgc(Ag+),pX=-lgc(X-),利用pX-pAg的坐标系可表示出 AgX的溶度积与溶液中的c(Ag+)和c(X-)的相互关系。下列说法错误的是
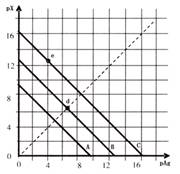
A.A线是AgCl,C线是AgI
B.e点表示由过量的KI与AgNO3反应产生AgI沉淀
C.d点是在水中加入足量的AgBr形成的饱和溶液
D.B线一定是AgBr
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com