
| A、钢管与铜管家露天堆放在一起,钢管不易腐蚀 |
| B、生铁浸泡在食盐水中发生析氢腐蚀 |
| C、给铁钉镀铜可采用CuSO4作电镀液 |
| D、电解饱和食盐水时在阳极得到氯气,阴极得到金属钠 |


科目:高中化学 来源: 题型:
| A、溶液的pH变大 |
| B、c(Na+)与c(CO32-)的比值变大 |
| C、溶液浓度变大,有晶体析出 |
| D、实质是电解水,有晶体析出 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、我们平时应多饮用很纯净的水,防止有毒物质进入体内 | ||
| B、所有天然水都不能饮用 | ||
C、人体内含有约
| ||
| D、人体需要不断补充水分,每人每天需要补充2.5~4L水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
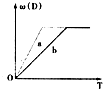 已知下列化学反应:3A(g)+B(g)?C(s)+4D(g)△H<0中a、b分别表示在一定条件下D的体积分数[ω(D)]随反应时间T的变化情况.若使曲线b变为曲线a,可采用的措施是( )
已知下列化学反应:3A(g)+B(g)?C(s)+4D(g)△H<0中a、b分别表示在一定条件下D的体积分数[ω(D)]随反应时间T的变化情况.若使曲线b变为曲线a,可采用的措施是( )| A、增大B的浓度 |
| B、升高温度 |
| C、缩小容器体积 |
| D、降低温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 有两个密闭容器A和B,在相同温度下,A保持恒压,B保持恒容.起始时两容器的体积相等,向A、B中分别通入2molSO2和1molO2,使之发生反应:2SO2+O2?2SO3,并达到平衡.
有两个密闭容器A和B,在相同温度下,A保持恒压,B保持恒容.起始时两容器的体积相等,向A、B中分别通入2molSO2和1molO2,使之发生反应:2SO2+O2?2SO3,并达到平衡.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、500mL2mol?L-1稀硫酸 |
| B、150mL5mol?L-1稍酸 |
| C、50mL3mol?L-1盐酸 |
| D、500mL2mol?L-1稀硫酸和少量硫酸铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、△H<0表示放热反应,△H>0表示吸热反应 |
| B、1molH2SO4与1molBa(OH)2反应放出的热叫中和热 |
| C、1molH2与0.5molO2反应放出的热就是H2的燃烧热 |
| D、热化学方程式中的化学计量数只表示物质的量,可以是分数 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、摩尔是一个基本物理量 |
| B、CH4的摩尔质量为16g |
| C、在同温同压下,相同体积的任何气体单质所含分子数相同 |
| D、500mL,1mol/L MgCl2溶液中含有Cl-数目为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
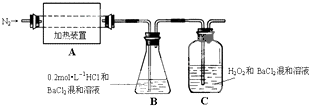 硫酸亚铁铵[(NH4)2Fe(SO4)2?6H2O]较硫酸亚铁不易被氧气氧化,是分析化学中重要的试剂,常用于代替硫酸亚铁.硫酸亚铁铵在 500℃时隔绝空气加热完全分解.回答下列问题:
硫酸亚铁铵[(NH4)2Fe(SO4)2?6H2O]较硫酸亚铁不易被氧气氧化,是分析化学中重要的试剂,常用于代替硫酸亚铁.硫酸亚铁铵在 500℃时隔绝空气加热完全分解.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com