
����Ŀ����֪�������ݣ�
���� | �۵�(��) | �е�(��) | �ܶ�(g��cm��3) |
�Ҵ� | ��117.0 | 78.0 | 0.79 |
���� | 16.6 | 117.9 | 1.05 |
�������� | ��83.6 | 77.5 | 0.90 |
ijѧ����ʵ������ȡ������������Ҫ�������£�
������2 mLŨ���ᡢ3 mL�Ҵ�(��18O)��2 mL����Ļ����Һ��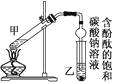
�ڰ���ͼ���Ӻ�װ��(װ������������)��������Һ����С����ȼ���3��5 min��
�۴��Թ����ռ���һ���������ֹͣ���ȣ������Թ��Ҳ�������Ȼ���ô��ֲ㡣
�ܷ��������������ϴ�ӡ����
��1�����Ƣ��л����Һ�ķ���Ϊ��
��Ӧ��Ũ�������������
д����ȡ���������Ļ�ѧ����ʽ����
��2������ʵ���б���̼������Һ��������________(����ĸ)��
A.�к�������Ҵ�
B.�к����Ტ�����Ҵ�
C.���������������ܽ�
D.�����������ɣ���������
��3�����������ҪС����ȼ��ȣ�����Ҫ��������
��������۲쵽����������
�������Թ��е����ʷ����Եõ���������������ʹ�õ�������������ʱ����������Ӧ������(��¿ڷš����Ͽڵ���)����
��4����ͬѧ����ʵ�飬�ó��Ҵ�������������͵õ��������������������±���
ʵ�� | �Ҵ�(mL) | ����(mL) | ���� |
�� | 2 | 2 | 1.33 |
�� | 3 | 2 | 1.57 |
�� | 4 | 2 | x |
�� | 5 | 2 | 1.76 |
�� | 2 | 3 | 1.55 |
��������x�ķ�Χ����ʵ��٢ڢ�̽��������
���𰸡�
��1����ŨH2SO4�����Ҵ��У��ӱ���Ȼ���������(���Ƚ��Ҵ��������Ϻ��ټ�Ũ���Ტ�ڼ�������в�����)����������ˮ����CH3COOH+CH3CH218OH![]() CH3CO18OCH2CH3+H2O
CH3CO18OCH2CH3+H2O
��2��B,C
��3�������Ȼᵼ�´�����ԭ����������ʧ�������ݲ�����Һ��ֲ㣬�ϲ�Ϊ��ɫ����ζҺ�壬�²�Ϊdz��ɫҺ�壬���²�Һ����ɫ��dz����Һ©�����Ͽڵ�
��4��1.57��1.76�������Ҵ�����������������IJ�����Ӱ��
��������(1)�����Ũ�����൱�ڱ�ϡ�ͣ���Ӧ��ŨH2SO4�����Ҵ��У�Ȼ��������ᣬҲ���Ƚ��Ҵ��������Ϻú��ټ���Ũ�����������Ӧ��������Ϊ���淴Ӧ��ʹ��Ũ����ɼӿ�������Ӧ�����ʲ�������ƽ�����������ķ����ƶ�(������ˮ)��������Ӧ�Ļ����������ǻ������⣬�����ɵ����к���18O��(2)ʹ�ñ���̼������Һ�������ǣ��ٿɳ�ȥ�������������е����ᣬ�������Ҵ����ڿɽ��������������ܽ�Ȳ�������Һ��ֲ㡣(3)�ɱ�������֪�Ҵ��ķе�(78.0��)�����������ķе�(77.5��)�ܽӽ������ô����ȣ��������Ҵ��ᱻ��������������ԭ�ϵĴ�����ʧ���������ܶ�С��ˮ���ܶȣ����ϲ�Ϊ��״����ζ����ɫҺ�壬�������һ��������������������������Na2CO3��Ӧ�����²�Һ���ɫ��dz�����ֲ��Һ����뿪����ʹ�÷�Һ©������Һʱ�ϲ�Һ��Ӧ���Ͽڵ�����(4)̽���Ҵ������������ĸı�������ʵ�Ӱ���������������ʵ������֪�������Ҵ�������������������������������ӡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������﮼��仯�����ڹ��ý�������;�㷺��ռ����Ҫ��λ��
��1�����Ԫ�����ڱ��е�λ����
��2������֤��﮵Ľ����������Ƶ�ʵ����ʵ��
��3����ͼ����ij���±ˮ����Ҫ��Na+��K+��Li+��Mg2+��Clһ�ȣ����еij�﮹���·��ͼ�� 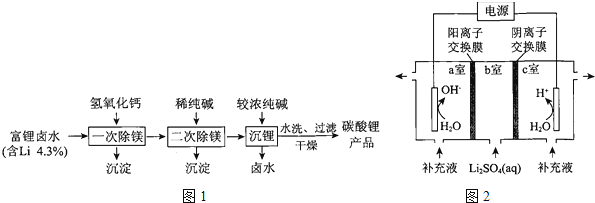
�١����γ�þ�����õij�������Ҫ�м�ʽ̼��þ��
�ڡ���ﮡ��͡����γ�þ��ʱ���ô����Ũ�Ȳ����ԭ����
��4���������Ʊ���̼��﮼������Ƶ��������Һ����������ͼ��ʾװ���Ʊ�������ﱣ�
��̼��������ᷴӦ�����ӷ���ʽ��
�ڽ�ϵ缫��Ӧʽ�����Ƶ�LiOH��ԭ����
�۸÷��п�ѭ�����õ������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2014��7��31���й����������ӱ�ʡ��չ������������ר�������ж���ǿ�������ϡ�������ij������������Ҫ�ɷ�ΪSiO2��MgO��Al2O3��Fe2O3�ȳɷ֣����շ����еĽ���Ԫ�صĹ���������ͼ��ʾ�� 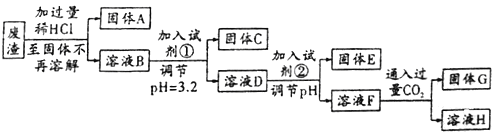
��֪�������£����Ͱ�ˮ��pHԼΪ11���������ӳ�������pH���������ʾ��
���� | ������������ʽ��ȫ����ʱ����pH | �������������ȫ�ܽ�ʱ����pH |
Fe3+ | 3.2 | |
A13+ | 5.3 | 11.9 |
Mg2+ | 12.3 |
��1���Լ���Ϊ �� �Լ���Ϊ��
A��AgNO3 B��NaOH C��NH3H2O D��H2SO4
��2������C�Ļ�ѧʽ�� �� ��ҺF�н���Ԫ�صĴ�����ʽΪ��
��3��д������A���Լ��ڷ�Ӧ�Ļ�ѧ����ʽ����F��ͨ�����CO2�����������ӷ���ʽΪ��
��4�������Լ��ڣ�ʵ����ҺD����ҺF��ת�����������Һ��pHΪ ��
A.6
B.10
C.12
D.13
��5��25��ʱ������4������pH������ҺF��c��Mg2+��=5.6��10��10mol/L����������þ��Ksp=��
��6�����һ����Ӧ���漰�������Σ�������ʽ�ε���Һ�и�����Ũ���ɴ�С��˳��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼʾװ����ȡ������������(�ƾ��Ƶ���ͼ�о�����ȥ)������գ�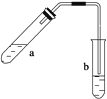
��1���Թ�a����Ҫ����Ũ���ᡢ��������Ҵ���2 mL����ȷ�ļ���˳�����ǣ�
��2��Ϊ��ֹa�е�Һ����ʵ��ʱ�������У��ڼ���ǰӦ��ȡ�Ĵ�ʩ�ǣ�
��3��ʵ���м����Թ�a��Ŀ���ǣ�
��4���Թ�b�м��б���Na2CO3��Һ���������ǣ�
��5����Ӧ���������Թ�b�����á��۲쵽�������ǣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶�ʱ��2L������X��Y��Z������̬���ʵ����ʵ�����n����ʱ�䣨t���仯��������ͼ��ʾ����ͼ�����ݷ����� 
��1���÷�Ӧ�Ļ�ѧ����ʽΪ�� ��
��2����Ӧ��ʼ��2min����Z��ʾ��ƽ����Ӧ����Ϊ�� ��
��3����������ʵ�У�ʲô����Ӱ���˻�ѧ��Ӧ�����ʣ� ��ͬŨ�ȡ�ͬ����������з����С��ͬ����Ƭ��þƬ���������п���������
���ۻ���KClO3�ų����ݺ�������������MnO2�ܿ�������壺 ��
��4�����ܱ������ͨ��a mol X��g����b mol Y��g����������ӦX��g��+Y��g��2Z��g�������ı���������ʱ����Ӧ���ʻᷢ��ʲô�仯����ѡ���������С�����䡱�� �������¶ȣ���Ӧ������
�ڱ�������������䣬���벻�μӷ�Ӧ�Ķ������壬��Ӧ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵���У�����ȷ���� (����)
A.�ִ�ҩ����Ҫ���˹��ϳɵ�ҩ��
B.��Ȼҩ��������õ�ҩЧ�����Բ���Ҫ���и���
C.ҩ���������Ը����Ľṹ�е�ijЩ�������й�
D.��ҩ�������������Ӧ��ǰ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A.�������ϵͳ����������Ϊ2����������
B.������������ȥ�����е���ϩ
C.�����м���ˮ������һ��ʱ���Һ�����ɫ��˵��������巢����ȡ����Ӧ
D.���м�������Ȼ�̼��Һ����Һ�ֲ㣬�ϲ�ʳȺ�ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ԫ�����ڱ���������������ȷ����( )
A. ���ڱ��е�15��Ԫ�ص�����������Ӧˮ����Ļ�ѧʽ��ΪH3RO4
B. ��������Ԫ�صļ���������������������������
C. �ڢ������������У���Ԫ������������
D. O22����S2��������ͬ���������͵�����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com