
在某一容积为2L的密闭容器内,加入0.8mol的H2和0.6mol的I2,在一定的条件下发生如下反应:H2(g)+I2(g)⇌2HI(g)△H<0反应中各物质的浓度随时间变化情况如图1:
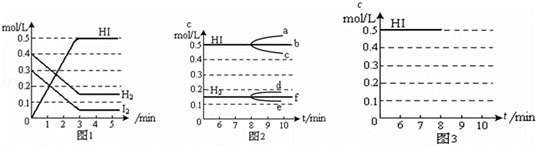
(1)该反应的化学平衡常数表达式为K= .
(2)反应达到平衡后,第8分钟时:
①若升高温度,化学平衡常数K (填写“增大”、“减小”或“不变”)HI浓度的变化正确的是 (用图2中a﹣c的编号回答)
②若加入I2,H2浓度的变化正确的是 ,(用图2中d﹣f的编号回答)
(3)反应达到平衡后,第8分钟时,若反应容器的容积扩大一倍,请在图3中画出8分钟后HI浓度的变化情况.
考点: 化学平衡的计算.
分析: (1)根据平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积进行计算;
(2)①根据化学平衡常数K只与温度有关,温度改变,若平衡正向移动,化学平衡常数K增大,生成物浓度增大,反之,若平衡逆向移动,化学平衡常数K减少,生成物浓度减少;
②若加入I2,平衡正向移动,H2浓度减少;
(3)反应是体积不变的反应,改变压强平衡不动,容器的容积扩大一倍,平衡物质浓度减小.
解答: 解:(1)平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积,所以平衡常数K= ,故答案为:K=
,故答案为:K= ;
;
(2)①该反应放热,升高温度,平衡逆向移动,化学平衡常数K减小,生成物浓度减少,故答案为:减小;c;
②若加入I2,平衡正向移动,H2浓度减少,故答案为:e;
(3)H2(g)+I2(g)⇌2HI(g),反应是体积不变的反应,改变压强平衡不动,容器的容积扩大一倍,平衡物质浓度减小,碘化氢浓度减小一半为0.25mol/L,画出的变化图象如图: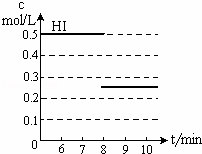 ,故答案为:
,故答案为: .
.
点评: 本题主要考查了平衡常数、化学平衡移动以及化学反应速率的计算,难度不大,需要注意的是:化学平衡常数K只与温度有关,温度改变,若平衡正向移动,化学平衡常数K增大,反之则减少.


科目:高中化学 来源: 题型:
在一个容积为2L的密闭容器中,发生如下反应:3X(气)+Y(气)═2Z(气),若最初加入的X、Y和Z都是1mol,反应中X的平均反应速率为0.12mol•L﹣1•s﹣1.若要产物Z为1.8mol,反应所需的时间为()
A. 5s B. 10s C. 15s D. 20s
查看答案和解析>>
科目:高中化学 来源: 题型:
科学家利用太阳能分解水生成的氢气在催化剂作用下与CO2反应生成甲醇(CH3OH),并开发出直接以甲醇为燃料的燃料电池.已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为﹣285.8kJ/mol、﹣283.0kJ/mol和﹣726.5kJ/mol,请回答下列问题:
(1)用太阳能分解5mol水消耗的能量是 kJ.
(2)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为 .
(3)已知25℃、101kPa下,H2O(l)═H2O(g)△H=+44kJ•mol﹣1.则1g甲醇(CH3OH)燃烧 生成CO2和气态水时放出的热量为 .
生成CO2和气态水时放出的热量为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上可利用合成气(CO和H2的混合气体)生产甲醇.已知:CO(g)+2H2(g)⇌CH3OH(g)△H=﹣92.9kJ/mol一定条件下,该反应在一体积固定的密闭容器中达到平衡.下列说法正确的是()
A. 该反应的△S<0
B. 该反应在任何温度下均能自发进行
C. 向容器中充入少量He,平衡向正反应方向移动
D. 升高温度平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
目前,科学家正在研究开发一种高能电池﹣﹣钠硫电池,它以熔融钠、硫为两极,以导电的β﹣A2lO3陶瓷作固体电解质,反应式如下:Na2SX 2Na+xS以下说法正确的是()
2Na+xS以下说法正确的是()
A. 放电时,Na作正极,S极发生还原反应
B. 放电时,Na发生还原反应
C. 充电时,钠 极与外电源的正极相连
极与外电源的正极相连
D. 充电时,阳极发生的反应为:SX2﹣﹣2e=xS
查看答案和解析>>
科目:高中化学 来源: 题型:
某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是()
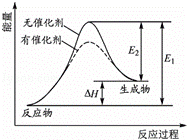
A. 该反应为吸热反应
B. 催化剂能改变反应的焓变
C. 催化剂能降低反应的活化能
D. 逆反应的活化能大于正反应的活化能
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应aA(g)+bB(g)⇌cC(g)+dD(g)符合图.则下列叙述正确的是()

A. a+b<c+d;正反应吸热 B. a+b>c+d;正反应放热
C. a+b<c+d;正反应放热 D. a+b>c+d;正反应吸热
查看答案和解析>>
科目:高中化学 来源: 题型:
1 L水中溶有Mg(HCO3)2和CaCl2的浓度分别是b mol·L-1和2b mol·L-1,现用一种试剂(适量)把Ca2+、Mg2+除去,这种试剂最好选用 ( )。
A.Ca(OH)2 B.NaOH
C.NaHCO3 D.Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
“类推”的思维方式在化学学习与研究中经常采用,但有时会产生错误结论.下列类推结论中,正确的是()
A. 由氢氟酸刻蚀玻璃可推知盐酸也能用来刻蚀玻璃
B. 由Na2O中阴阳离子个数比为1:2,可推出Na2O2中阴阳离子个数比为 1:1
C. 由钠与冷水剧烈反应,可推知钾也能与冷水剧烈反应
D. 由“2Fe+3Br2═2FeBr3”反应可推出“2Fe+3I2═2FeI3”反应也能发生
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com