
科目:高中化学 来源: 题型:
| 催化剂△ |
查看答案和解析>>
科目:高中化学 来源: 题型:038
某厂以硫铁矿为原料,用接触法制硫酸。硫铁矿煅烧时FeS2的利用率为90% ,SO2转化为SO3时转化率为95%,SO3被吸收时有2% SO3随尾气排出,现有含FeS2 70%的硫铁矿1t,可生产98%的硫酸多少吨?
查看答案和解析>>
科目:高中化学 来源: 题型:
(6分)某硫酸厂以硫铁矿为原料生产硫酸,主要过程的化学反应情况如下:
| 生产过程 | 化学反应 | 反应情况 |
| 硫铁矿的燃烧 | 4 +11O2 | 4%的硫元素损失而混入炉渣 |
| SO2的接触氧化 | 2SO2+O2 | SO2转化率为95% |
| SO3的吸收 | SO3+H2O=H2SO4 | SO3的吸收率为98% |
(1)将硫铁矿燃烧的化学方程式补充完整:4 +11O2![]() 2Fe2O3+8SO2
2Fe2O3+8SO2
(2)该厂现用100吨含硫40%的硫铁矿生产硫酸,可生产98%的浓H2SO4多少吨?(除上述硫的损失外,忽略其它损失)
查看答案和解析>>
科目:高中化学 来源:2013届湖北省春季高一下学期期中考试化学试卷 题型:填空题
(6分)某硫酸厂以硫铁矿为原料生产硫酸,主要过程的化学反应情况如下:
|
生产过程 |
化学反应 |
反应情况 |
|
硫铁矿的燃烧 |
4
+11O2 |
4%的硫元素损失而混入炉渣 |
|
SO2的接触氧化 |
2SO2+O2 |
SO2转化率为95% |
|
SO3的吸收 |
SO3+H2O=H2SO4 |
SO3的吸收率为98% |
(1)将硫铁矿燃烧的化学方程式补充完整:4
+11O2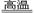 2Fe2O3+8SO2
2Fe2O3+8SO2
(2)该厂现用100吨含硫40%的硫铁矿生产硫酸,可生产98%的浓H2SO4多少吨?(除上述硫的损失外,忽略其它损失)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com