
����Ŀ����100��ʱ����0.40 mol NO2�������2 L���ܱ������У��������·�Ӧ��2NO2��g�� ![]() N2O4��g�� H < 0����ⷴӦ����������ݣ�
N2O4��g�� H < 0����ⷴӦ����������ݣ�
ʱ��/s | 0 | 20 | 40 | 60 | 80 |
n��NO2��/mol | 0.40 | n1 | 0.26 | n3 | n4 |
n��N2O4��/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
����˵����ȷ����
A��0~20 s�ڣ�v��NO2�� = 0.005 mol��L-1.s-1
B��59 sʱ��c��NO2��һ������0.12 mol��L-1
C����������ʼʱ����NO2��������0.80 mol����÷�Ӧ��ƽ�ⳣ��K > 25/9
D����������Ӧ��120��ʱ���У���Ӧ��80 sʱ��n��N2O4�� < 0.08 mol
���𰸡�D
��������
���������A��0~20 s�ڣ�v��N2O4����![]() ��0.00125 mol��L-1.s-1����Ӧ����֮���ǻ�ѧ������֮�ȣ���v ��NO2�� = 0.0025 mol��L-1.s-1��A����B��59 sʱ����ﵽƽ��״̬����c��NO2����
��0.00125 mol��L-1.s-1����Ӧ����֮���ǻ�ѧ������֮�ȣ���v ��NO2�� = 0.0025 mol��L-1.s-1��A����B��59 sʱ����ﵽƽ��״̬����c��NO2����![]() =0.12 mol��L-1������Ӧ��һ����ƽ��״̬��B����C��
=0.12 mol��L-1������Ӧ��һ����ƽ��״̬��B����C��
2NO2��g�� ![]() N2O4��g��
N2O4��g��
��ʼŨ����mol/L�� 0.2 0
ת��Ũ����mol/L�� 0.08 0.04
ƽ��Ũ����mol/L�� 0.12 0.04
���Ը��¶���ƽ�ⳣ��K��![]()
ƽ�ⳣ��ֻ���¶��й�ϵ��������������ʼʱ����NO2��������0.80 mol����÷�Ӧ��ƽ�ⳣ��K �� 25/9��C����D������Ӧ�Ƿ��ȷ�Ӧ�������¶�ƽ�����淴Ӧ������У�������������Ӧ��120��ʱ���У���Ӧ��80 sʱ��n��N2O4�� < 0.08 mol��D��ȷ����ѡD��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ���������������෨����ij����ʱ������Һ�������˶��ֱ��軯ѧԪ�ء����䷽���£�
�롡�� | K�� | Na�� | Mg2�� | Ca2�� | NO3- | H2PO4- | SO32- | Zn2�� |
����ҺŨ��/mol��L��1 | 1 | 0.25 | 1 | 2 | 1 | 0.25 | 1 |
���л��ܸ�ϸ���������ٵ�������
A. Ca2�� B. Zn2�� C. SO32- D. H2PO4-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ���ܴﵽĿ�ĵ��ǣ� ��
A�����Ҵ���Ũ�����ȥ���������е���������
B����NaOH��Һ��FeCl3��Һ�Ʊ�Fe(OH)3����
C����Ʒ����������Na2SO3��Na2CO3
D����������ϩ��SO2ͨ������KMnO4��Һ�г�ȥ��ϩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������β���ﺬ�е�NO������������ȼ��ȼ�յĸ�����������������Ӧ���£�N2(g)��O2(g)![]() 2NO(g)��H��0����֪�÷�Ӧ��2404��ʱ��ƽ�ⳣ��K��64��10��4����ش�
2NO(g)��H��0����֪�÷�Ӧ��2404��ʱ��ƽ�ⳣ��K��64��10��4����ش�
��1��ij�¶��£���2 L���ܱ������г���N2��O2��1 mol��5���Ӻ�O2�����ʵ���Ϊ0.5 mol����N2�ķ�Ӧ����Ϊ_________________��
��2���ٶ��÷�Ӧ���ں��������½��У��жϸ÷�Ӧ�ﵽƽ��״̬�ı�־__________��
A������1 mol N2ͬʱ����1 mol O2 B����������ܶȲ���
C���������ƽ����Է����������� D��2v��(N2)��v��(NO)
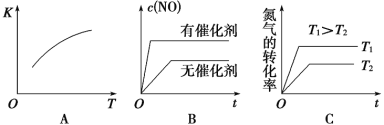
��3����N2��O2�Ļ�����������º����ܱ������У���ͼ�仯������ȷ����________(����ĸ���)��
��4������º��ݵ��ܱ������г�������ʵ�����N2��O2���ﵽƽ��״̬���������г���һ����NO�����´ﵽ��ѧƽ��״̬����ԭƽ��״̬��ȣ���ʱƽ��������NO���������________��(���������������С������������)
��5�����¶��£�ijʱ�̲��������N2��O2��NO��Ũ�ȷֱ�Ϊ2.5��10��1 mol/L��4.0��10��2 mol/L��3.0��10��3 mol/L����ʱ��Ӧ_____________(�������ڻ�ѧƽ��״̬������������Ӧ����������������淴Ӧ���������)��������_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����·�Ӧ�ᵼ����Һ�����Լ��������Ե���( )
A. Na2SO4��Һ����BaCl2����
B. Ba(OH)2��Һ�м���CuSO4(����)����
C. NaOH��Һͨ��HCl
D. H2O���NaCl����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ʾ��װ�ã�C��D��E��F��X��Y���Ƕ��Ե缫������ؽ�ͨ�������е����̪��Һ����F��������Һ�Ժ�ɫ��������˵����ȷ����
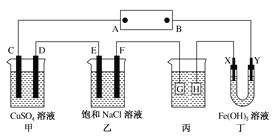
A����ԴB��������
B���ס���װ�õ�C��D��E��F�缫���е������ɣ������ʵ���֮��Ϊ1��2��2��1
C�����ñ�װ�ø�ͭ������HӦ����Ag�����Һ��AgNO3��Һ
D��װ�ö���Y���������ɫ���˵���������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڹ̶�������ܱ������н��е����巴Ӧ����˵��A(g) + B��g��![]() C��g��+D��g���ں������Ѵﵽƽ�����
C��g��+D��g���ں������Ѵﵽƽ�����
A����Ӧ������ѹǿ����ʱ����仯
B��A�����B����������������
C��A��B��C��������������������
D����Ӧ���������ܶȲ���ʱ����仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����õ�ⷨ�ɽ�����Fe��Zn��Ag��Pt�����ʵĴ�ͭ�ᴿ������������ȷ����( )
A�����ʱ�Ծ�ͭ������
B�����ʱ��������������Ӧ
C����ͭ���ӵ�Դ��������缫��Ӧ��Cu��2e��=Cu2��
D�������۵ײ����γɺ�����Ag��Pt�Ƚ�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������NaOH��BaCl2��Al2��SO4��3���ֹ�����ɵĻ��������������ˮ��,����ܽ��,������Һ�еμ�1mol��L-1��ϡ����,����ϡ�������������ɳ�����������ϵ��ͼ��ʾ�������й��ж���ȷ������ ��
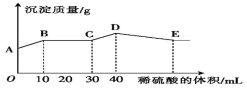
A.AB�η�����Ӧ�����ӷ���ʽΪBa2++SO42-=BaSO4��
B.BC�η�����Ӧ�����ӷ���ʽΪH++OH-=H2O
C.D���ʾ�ij����Ļ�ѧʽΪAl��OH��3
D.E��ʱ��Һ�к��д�����AlO2-
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com