
| A.浓硫酸滴在润湿的蓝色石蕊试纸上,试纸先变红,然后褪色,最后变黑,说明浓硫酸具有酸性、氧化性和吸水性 |
B.样品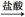 无明显现象 无明显现象 出现白色沉淀,说明样品中含SO42- 出现白色沉淀,说明样品中含SO42- |
| C.常温下浓硫酸能用铁制容器盛装,说明浓硫酸与Fe不反应 |
| D.样品中加入盐酸得到使澄清石灰水变浑浊的气体,说明样品中含CO32-或HCO3- |
 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源:不详 题型:单选题
| A.用过滤法分离氢氧化铁胶体和三氯化铁溶液的混合物 |
| B.用容量瓶配制溶液,定容后摇匀液面下降,再加蒸馏水至刻度线配制溶液浓度 |
| C.向含有少量Ca(OH)2的Mg(OH)2悬浊液中加入饱和MgCl2溶液,充分搅拌后过滤,洗涤,可达到除去Mg(OH)2中的少量Ca(OH)2的目的 |
| D.将金属钠投入到足量CuSO4溶液中,静置后溶液质量增加 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用苯萃取碘水中的碘时,应先打开上端玻璃塞再将苯层从分液漏斗下口放出 |
| B.用湿润的红色石蕊试纸检验氨气 |
| C.稀释浓硫酸时,应将浓硫酸沿玻璃棒缓慢注入盛水的量筒中 |
| D.用广泛pH试纸测得0.1 mol·L-1 NH4Cl溶液的pH=5.2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
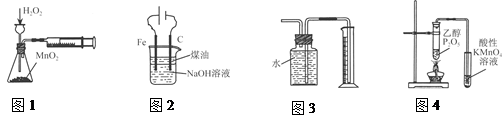
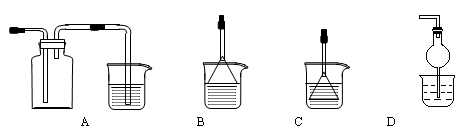
| A.图1定量测定H2O2的分解速率 |
| B.图2装置制备Fe(OH)2并能较长时间观察其颜色 |
| C.图3装置测量Cu与浓硝酸反应产生气体的体积 |
| D.图4证明CH3CH2OH发生消去反应生成了乙烯 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
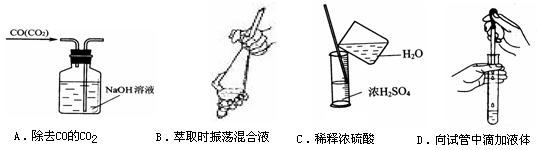
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗 |
| B.当出现CO中毒时,应立即将中毒者抬到室外新鲜空气处 |
| C.制取并排水法收集氧气结束后,应立即停止加热 |
| D.将含硫酸的废液倒入水槽,用水冲人下水道 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
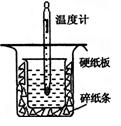
| 温度 实验次数 | 起始温度t1℃ | 终止温度t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 29.5 | |
| 2 | 27.0 | 27.4 | 27.2 | 32.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.2 | |
| 4 | 26.4 | 26.2 | 26.3 | 29.8 | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
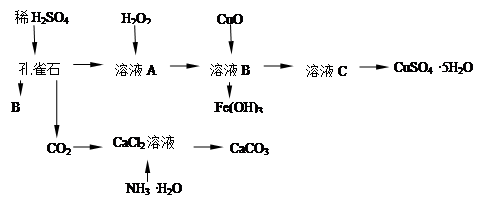
| A.KMnO4溶液 | B.Fe粉 | C.Na2CO3溶液 | D.KSCN溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com