铜、铁都是日常生活中常见的金属,它们的单质及其化合物在科学研究和工农业生产中具有广泛用途.
请回答以下问题:
(1)超细铜粉可用作导电材料、催化剂等,其制备方法如下:
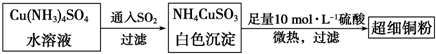
①Cu
2+的价电子排布图
; NH
4CuSO
3中N、O、S三种元素的第一电离能由大到小顺序为
(填元素符号).
②SO
42-的空间构型为
,SO
32-离子中心原子的杂化方式为
.
(2)请写出向Cu(NH
3)
4SO
4水溶液中通入SO
2时发生反应的离子方程式:
.
(3)某学生向CuSO
4溶液中加入少量氨水生成蓝色沉淀,继续加入过量氨水沉淀溶解,得到深蓝色透明溶液,最后向该溶液中加入一定量乙醇,析出[Cu(NH
3)
4]SO
4?H
2O晶体.
①下列说法正确的是
a.氨气极易溶于水,是因为NH
3分子和H
2O分子之间形成3种不同的氢键
b.NH
3分子和H
2O分子,分子空间构型不同,氨气分子的键角小于水分子的键角
c.Cu(NH
3)
4SO
4所含有的化学键有离子键、极性共价键和配位键
d.Cu(NH
3)
4SO
4组成元素中电负性最大的是氮元素
②请解释加入乙醇后析出晶体的原因
.
(4)Cu晶体的堆积方式如图所示,设Cu原子半径为r,晶体中Cu原子的配位数为
,晶体的空间利用率为
(
≈1.4,列式并计算结果).




 ;N、O、S三种元素中由于N原子的2p轨道是半充满状态,所以第一电离能最大;同主族元素,随电子层数的增多,第一电离能逐渐减小;
;N、O、S三种元素中由于N原子的2p轨道是半充满状态,所以第一电离能最大;同主族元素,随电子层数的增多,第一电离能逐渐减小; ;N、O、S三种元素中由于N原子的2p轨道是半充满状态,所以第一电离能最大;同主族元素,随电子层数的增多,第一电离能逐渐减小,所以3种元素的第一电离能由大到小顺序为:N>O>S;
;N、O、S三种元素中由于N原子的2p轨道是半充满状态,所以第一电离能最大;同主族元素,随电子层数的增多,第一电离能逐渐减小,所以3种元素的第一电离能由大到小顺序为:N>O>S; ,N>O>S;
,N>O>S;

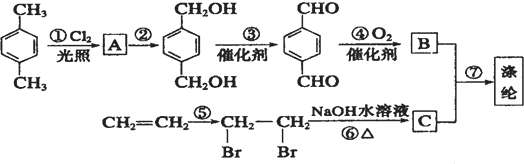


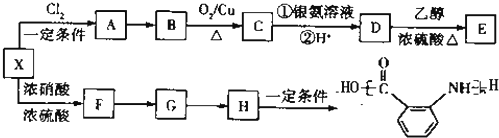
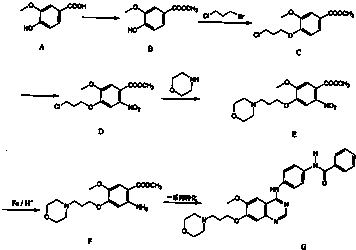
 )为原料合成对氨基苯甲酸乙酯(
)为原料合成对氨基苯甲酸乙酯(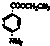 )的合成路线(试剂任选,用合成路线流程图表示)
)的合成路线(试剂任选,用合成路线流程图表示)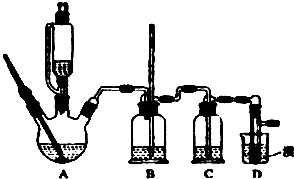 实验室制备1,2-二溴乙烷的反应原理如下:CH3CH2OH
实验室制备1,2-二溴乙烷的反应原理如下:CH3CH2OH