
A.CH4+2O2 CO2+2H2O CO2+2H2O | B.2H2+O2 2H2O 2H2O |
| C.HNO3+NaOH=NaNO3+ H2O | D.CuSO4+Fe=" Cu" +Fe SO4 |
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.该电池工作时,正极反应为:2AgCl+2e-=2Cl-+2Ag |
| B.镁电极作该电池负极,负极反应为:Mg-2e-=Mg2+ |
| C.当有24g Mg被氧化时,有108 g Ag被还原 |
| D.装备该电池的鱼雷在水中行进时,海水作为电解质溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 AsO33-+I2+H2O,设计如下图装置,进行下述操作:
AsO33-+I2+H2O,设计如下图装置,进行下述操作: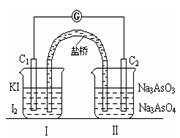
| A.①操作过程中C1棒上发生的反应为2I--2e-=I2 |
| B.②操作过程中导线上电子定向移动方向由C2→C1 |
| C.若将微安表换成电解冶炼铝装置,在②操作过程中与C2棒连接的电极上产生氧气 |
| D.若将微安表换成电解饱和食盐水装置以模拟氯碱工业,在①操作过程中与C1棒连接的可以是Pt-Fe合金电极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
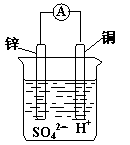
| A.Zn2++ 2e一 =Zn | B.2H++2e一= H2 ↑ |
| C.Zn一2e一=Zn2+ | D.Cu2++2e一= Cu |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

| A.金属活动性铝比镁强 |
| B.金属活动性镁比铝强,两装置中镁均为负极 |
| C.仅根据金属活动性顺序不能准确判断原电池的正负极 |
| D.原电池中的正负极受电解质溶液的酸碱性、强氧化性等因素的影响 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com