
【题目】化学与我们的生产生活联系紧密,下列有关说法不正确的是( )
A. 人工固氮过程和乙酸乙酯的制备反应均为有限度的
B. 用漂白粉进行泳池消毒和用铁罐保存冷的浓硫酸都利用了化学物质的强氧化性
C. 高炉炼铁和用粮食酿酒的化学反应中都有二氧化碳生成
D. 豆浆的丁达尔效应和肥皂的去污过程发生的均为化学变化
【答案】D
【解析】
A. 人工固氮过程发生的反应为:N2+3H2![]() 2NH3,乙酸乙酯的制备过程发生的反应为:CH3COOH+CH3CH2OH
2NH3,乙酸乙酯的制备过程发生的反应为:CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O,两者均为可逆反应,反应有限度,A项正确;
CH3COOCH2CH3+H2O,两者均为可逆反应,反应有限度,A项正确;
B. 用漂白粉进行泳池消毒,主要是因为漂白粉反应生成的次氯酸具有强氧化性;用铁罐保存冷的浓硫酸是由于浓硫酸具有强氧化性,在常温下铁遇浓硫酸会发生钝化现象,B项正确;
C. 高炉炼铁的方程式为:3CO + Fe2O3![]() 3CO2 +2Fe;用粮食酿酒的主要化学反应为:淀粉先转化为葡萄糖,葡萄糖经发酵作用再转化为酒精和二氧化碳,C项正确;
3CO2 +2Fe;用粮食酿酒的主要化学反应为:淀粉先转化为葡萄糖,葡萄糖经发酵作用再转化为酒精和二氧化碳,C项正确;
D. 豆浆的丁达尔效应利用的是胶体的物理性质,肥皂的去污过程主要涉及通过肥皂分子的亲水端溶解在水中、而亲油端进入油污团块的内部,从而松动油污,把它们稀释、扩散、乳化、洗掉,不涉及化学变化,D项错误;
答案选D。


科目:高中化学 来源: 题型:
【题目】二氧化碳的捕集与利用是实现温室气体减排的重要途径之一。
(1)目前工业上使用的捕碳剂有 NH3 和(NH4)2CO3,它们与 CO2 可发生如下可逆反应:
2NH3(l)+H2O(l)+CO2(g) ![]() (NH4)2CO3(aq) K1
(NH4)2CO3(aq) K1
NH3(l)+H2O(l)+CO2(g) ![]() NH4HCO3(aq) K2
NH4HCO3(aq) K2
(NH4)2CO3(aq)+H2O(l)+CO2(g) ![]() 2NH4HCO3(aq) K3
2NH4HCO3(aq) K3
则 K3=________(用含 K1、K2 的代数式表示)。
(2)利用 CO2 制备乙烯是我国能源领域的一个重要战略方向,具体如下:
方法一:
CO2 催化加氢合成乙烯,其反应为:2CO2(g)+6H2(g) ![]() C2H4(g)+4H2O(g) △H=a kJ·mol-1起始时按 n(CO2)∶n(H2)=1∶3的投料比充入20 L的恒容密闭容器中,不同温度下平衡时H2和H2O的物质的量如图甲所示:
C2H4(g)+4H2O(g) △H=a kJ·mol-1起始时按 n(CO2)∶n(H2)=1∶3的投料比充入20 L的恒容密闭容器中,不同温度下平衡时H2和H2O的物质的量如图甲所示:

①a______0(选填“>”或“<”)。
②下列说法正确的是______(填字母序号)。
A 、使用催化剂,可降低反应活化能,加快反应速率
B 、其它条件不变时,若扩大容器容积,则 v正减小,v逆增大
C 、测得容器内混合气体密度不随时间改变时,说明反应已达平衡
③393 K下,H2的平衡转化率为________(保留三位有效数字)。
④393 K下,该反应达到平衡后,再向容器中按 n(CO2)∶n(H2)=1∶3 投入 CO2 和 H2 ,则n(H2)/n(C2H4)将____(填“变大”、“不变”或“变小”)。
方法二:
用惰性电极电解强酸性的二氧化碳水溶液可得到乙烯,其原理如图乙所示。
⑤b电极上的电极反应式为_______。
⑥该装置中使用的是__________(填“阴”或“阳”)离子交换膜。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某试液中只可能含有K+、NH4+、Fe2+、Al3+、Cl-、SO42-、CO32-、AlO2-中的若干种离子,离子浓度均为0.1mol/L,某同学进行了如下实验:

下列说法正确的是
A. 无法确定原试液中是否含有Al3+、Cl-
B. 滤液X中大量存在的阳离子有NH4+、Fe2+和Ba2+
C. 原溶液中存在的离子为NH4+、Fe2+、Cl-、SO42-
D. 无法确定沉淀C的成分
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列能用勒夏特列原理解释的是( )
A. 铁在潮湿的空气中易腐蚀
B. H2、I2、HI平衡混和气加压后颜色变深
C. 往往需要在催化剂条件下SO2氧化成SO3
D. 棕红色NO2加压后颜色先变深后变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的装置,C、D、E、F、X、Y都是惰性电极,将电源接通后,向(乙)中滴入酚酞溶液,在F极附近显红色,则以下说法正确的是

A. 电源B极是正极
B. 装置(丁)中X极附近红褐色变深,说明氢氧化铁胶粒带正电荷
C. 欲用(丙)装置给铜镀银,H应该是Ag,电镀液是AgNO3溶液
D. (甲)、(乙)装置的C、D、E、F电极均有单质生成,其物质的量之比为1 : 2 : 2 : 2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C三种烃,其球棍模型如下图:
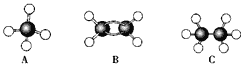
(1)等质量的以上物质完全燃烧时耗去O2的量最多的是________(填对应字母,下同);
(2)同状况、同体积的以上三种物质完全燃烧时耗去O2的量最多的是____________;
(3)等质量的以上三种物质燃烧时,生成二氧化碳最多的是________,生成水最多的是________。
(4)在120℃、1.01×105 Pa下时,有两种气态烃和足量的氧气混合点燃,相同条件下测得反应前后气体体积没有发生变化,这两种气体是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下实验方案合理的是( )
实验目的 | 实验设计 | |
A | 鉴别乙醇和二甲醚 | 分别取少量样品用元素分析仪进行测定 |
B | 用高锰酸钾溶液滴定未知浓度的乙二酸溶液 | 用待装液体分别润洗酸式和碱式滴定管再进行操作 |
C | 确定某无色溶液中含有 | 取少量待测液加 |
D | 鉴别 | 分别滴加氨水至过量,观察现象 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.按如图所示装置进行实验,并回答下列问题:

(1)甲池,通入CH3OH(甲醇)的电极反应式为______________________。
(2)乙池中的总反应化学方程式为______________________。
(3)当甲池中消耗O20.56L(标准状况下)时,理论上乙池中B极的质量增加__________g;此时丙装置中___________(填“c”或“d”)电极折出1.20g金属,则按丙装置中的的某盐溶液可能是__________________(填序号)。
a.MgSO4溶液 b.CuSO4溶液 c.NaCl溶液 d.AgNO3溶液
Ⅱ.SO2、CO、CO2、NOx是对环境影响较大的几种气体,对它们的合理控利和治理是优化我们生存环境的有效途径。

(4)利用化学原理将C0、SO2转化为重要化工原料,装置如图所示:
①若A为CO,B为H2,C为CH3OH,则通入CO一极为____________________极。
②若A为SO2,B为O2,C为H2SO4,则负极的电极反应式为____________________。
③若A为NO2,B为O2,C为HNO3,则正极的电极反应式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】离子反应广泛用于化学研究、工业生产、食品检验、环境保护等方面。
(1)向0.01mol·L-1 Ba(OH)2溶液中匀速逐滴加入0.01mol·L-1 H2SO4溶液直至过量,整个过程中混合溶液的导电能力(用I表示)可近似地用下图中的____________(填字母)曲线表示,发生反应的离子方程式为__________________________________。

(2)提纯后的粗盐中,还含有MgCl2、Na2SO4和CaCl2等可溶性杂质,欲通过下列流程得到较纯净的NaCl固体。

①操作a、操作d均用到玻璃棒,作用分别是____________、____________。
②固体Ⅲ是________(填化学式),加入过量Z溶液的目的是________________。
③操作e的名称是____________________。
④检验制得的NaCl晶体中是否含有Na2SO4的方法是__________________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com