
【题目】硼酸(H3BO3)为一元弱酸,H3BO3可以通过电解的方法制备。其工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过)。下列说法错误的是
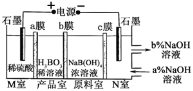
A.b膜为阴离子交换膜
B.阳极的电极反应式为:2H2O-4e- = O2↑+4H+
C.N室中:a%<b%
D.理论上每生成1mol产品,阴极室可生成5.6L(标准状况)气体
【答案】D
【解析】
由题意可知,通过电解NaB(OH)4溶液的方法制备硼酸,右边为阴极室,发生还原反应,2H2O+2e- = H2↑+2OH-,左边为阳极室,发生氧化反应2H2O-4e- = O2↑+4H+。故a为阳离子交换膜,b为阴离子交换膜,c为阳离子交换膜,所以反应后NaOH溶液浓度变大。根据此分析进行解答。
A.由题意可知,b为阴离子交换膜,H+与NaB(OH)4在产品室反应生成硼酸(H3BO3)和水,故A选项正确。
B.阳极室,发生氧化反应2H2O-4e- = O2↑+4H+,故B选项正确。
C.N室中发生还原反应生成OH-,反应以后NaOH溶液浓度变大,故a%<b%,故C选项正确。
D.每生成1mol产品,转移1mol电子,阴极室可生成0.5mol H2,为11.2L(标准状况)气体,故D选项错误。
故答案选D。


科目:高中化学 来源: 题型:
【题目】一定温度下,在某体积固定的密闭容器中加入2 mol A和1 mol B,发生可逆反应![]() ,下列说法正确的是
,下列说法正确的是
A. 当容器内压强不变时说明反应已达到平衡
B. 当反应达到平衡时:c(A):c(B):c(C)=2:1:3
C. 当反应达到平衡时放出热量akJ
D. 其他条件不变,升高温度反应速率加快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气是重要的化工原料,工业上由N2和H2在一定条件下合成。
(1)已知H2的标准燃烧热为△H1=-akJ·mol-1,NH3的标准燃烧热为△H2=-bkJ·mol-1。则合成氨反应:N2(g)+3H2(g)![]() 2NH3(g)的△H3=_________ kJ·mol-1 (用含a、b的代数式表示)。
2NH3(g)的△H3=_________ kJ·mol-1 (用含a、b的代数式表示)。
(2)合成氨反应:N2(g)+3H2(g) ![]() 2NH3(g)在一定温度下能自发进行,则△H3______0(填“>”或“<”),原因是__________。
2NH3(g)在一定温度下能自发进行,则△H3______0(填“>”或“<”),原因是__________。
(3)一定温度下,向体积为2L的密闭容器中通入一定量的N2和H2反生反应,有关物质的量随反应时间的变化如图所示。该温度下,反应的平衡常数为_________________。
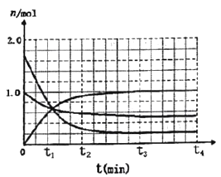
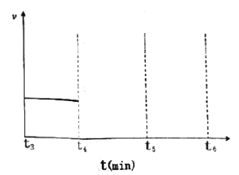
若在t4时刻,同时向体系中再通入0.5 mol N2和1moNH3,t5时刻重新达到平衡,请在下图中画出t4~t6时间段逆反应速率随时间的变化图_____________。
(4)文献报道,常压下把氢气和用氦气稀释的氮气分别通入一个加热到570℃的电解池中,采用高质子导电性的SCY陶瓷(能传递H+)为介质可在电极上直接生成氨气。阴极的反应方程式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,将3 mol A气体和1 mol B气体混合于固定容积为2 L的密闭容器中,发生反应:3A(g)+B(g) ![]() C(g)+2D(s)。2 min末该反应达到平衡,生成D的物质的量随时间的变化情况如图所示。下列判断正确的是( )
C(g)+2D(s)。2 min末该反应达到平衡,生成D的物质的量随时间的变化情况如图所示。下列判断正确的是( )
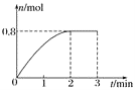
A. 若混合气体的密度不再改变时,该反应不一定达到平衡状态
B. 2 min后,加压会使正反应速率加快,逆反应速率变慢
C. 反应过程中A和B的转化率之比为3∶1
D. 开始到平衡,用A表示的化学反应速率为0.3 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2L的密闭容器中,X、 Y、Z三种气体的物质的量随时间变化的曲线如图所示:

下列描述正确的是( )
A. 反应开始到10s,用Z表示的反应速率为0.158mol/(L·s)-1
B. 反应开始到l0s,X的物质的量浓度减少了0.79mol/L
C. 反应开始到10s时,Y的转化率为79.0%
D. 反应的化学方程式为:X(g)+Y(g)![]() Z(g)
Z(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知充分燃烧a g乙炔(C2H2)气体时生成1 mol二氧化碳气体和液态水,并放出热量b kJ,则表示乙炔燃烧热的热化学方程式正确的是( )
A.2C2H2(g)+5O2(g) =4CO2(g)+2H2O(g) ΔH=-4b kJ·mol-1
B.C2H2(g)+![]() O2(g) =2CO2(g)+H2O(l) ΔH=-2b kJ·mol-1
O2(g) =2CO2(g)+H2O(l) ΔH=-2b kJ·mol-1
C.C2H2(g)+![]() O2(g) =2CO2(g)+H2O(g) ΔH=+2b kJ·mol-1
O2(g) =2CO2(g)+H2O(g) ΔH=+2b kJ·mol-1
D.2C2H2(g)+5O2(g) =4CO2(g)+2H2O(l) ΔH=+4b kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种制备高效漂白剂NaClO2的实验流程如图所示,反应I中发生的反应为3NaClO3+4SO2+3H2O====2ClO2+Na2SO4+3H2SO4+NaCl,下列说法中正确的是
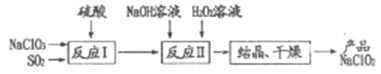
A. 反应Ⅱ中H2O2做还原剂
B. 产品中含有SO42-、Cl-
C. NaClO2的漂白原理与SO2相同
D. 实验室进行结晶操作通常在坩埚中进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家设计了一种可以循环利用人体呼出的CO2并提供O2的装置,总反应方程式为2CO2=2CO+O2。下列说法正确的是( )
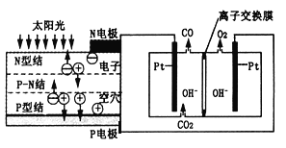
A. 由图分析N电极为电池的正极
B. 阴极的电极反应为CO2+H2O+2e-=CO+2OH-
C. OH-通过离子交换膜迁向左室
D. 反应完毕,该装置中电解质溶液的碱性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如下所示。下列说法错误的是
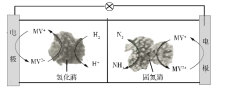
A. 相比现有工业合成氨,该方法条件温和,同时还可提供电能
B. 阴极区,在氢化酶作用下发生反应H2+2MV2+![]() 2H++2MV+
2H++2MV+
C. 正极区,固氮酶为催化剂,N2发生还原反应生成NH3
D. 电池工作时质子通过交换膜由负极区向正极区移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com