
【题目】(1)氢能源是绿色燃料,可以减少汽车尾气的排放,利用甲醇与水蒸气反应可以制备氢气:CH3OH(g)+H2O(g)===CO2(g)+3H2(g)。下图是该反应的能量变化图:

①通过图中信息可判断反应CH3OH(g)+H2O(g)===CO2(g)+3H2(g)的ΔH________0(选填“>”“=”或“<”)。
②图中途径(Ⅱ)的条件是__________________,途径(Ⅰ)的反应热________途径(Ⅱ)的反应热(选填“>”“=”或“<”)。
③在25 ℃、101 kPa下,1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ。则表示甲醇燃烧热的热化学方程式为__________________________________________。
(2)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。已知:
①2NH3(g)+CO2(g)===NH2CO2NH4(s) ΔH=-159.5 kJ/mol
②NH2CO2NH4(s)===CO(NH2)2(s)+H2O(g) ΔH=+116.5 kJ/mol
③H2O(l)===H2O(g) ΔH=+44.0 kJ/mol
写出CO2与NH3合成尿素和液态水的热化学反应方程式__________________。
【答案】 > 催化剂 = CH3OH(1)+3/2O2(g)===CO2(g)+2H2O(1) ΔH=-725.76 kJ·mol-1 2NH3(g)+CO2(g)===CO(NH2)2(s)+H2O(l) ΔH=-87.0 kJ/mol
【解析】(1)①通过图中信息可知反应物总能量 生成物总能量,因此反应CH3OH(g)+H2O(g)===CO2(g)+3H2(g)的ΔH>0。②图中途径(Ⅱ)的活化能减小,因此条件是使用了催化剂,催化剂改变活化能,不能改变反应热,因此途径(Ⅰ)的反应热等于途径(Ⅱ)的反应热;③在25 ℃、101 kPa下,1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ。则1mol甲醇即32g甲醇完全放出的热量是22.68 kJ×32=725.76 kJ,由于在一定条件下,1mol可燃物完全燃烧生成稳定氧化物时所放出的热量是燃烧热,因此表示甲醇燃烧热的热化学方程式为CH3OH(1)+3/2O2(g)===CO2(g)+2H2O(1) ΔH=-725.76 kJ·mol-1。(2)已知:
①2NH3(g)+CO2(g)===NH2CO2NH4(s) ΔH=-159.5 kJ/mol
②NH2CO2NH4(s)===CO(NH2)2(s)+H2O(g) ΔH=+116.5 kJ/mol
③H2O(l)===H2O(g) ΔH=+44.0 kJ/mol
则根据盖斯定律可知①+②-③即得到CO2与NH3合成尿素和液态水的热化学反应方程式为2NH3(g)+CO2(g)===CO(NH2)2(s)+H2O(l) ΔH=-87.0 kJ/mol。


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源: 题型:
【题目】粗硅提纯常见方法之一是先将粗硅与HCl反应制得SiHCl3,经提纯后再用H2还原:SiHCl3(g)+H2(g) ![]() Si(s)+3HCl(g)。在2L密闭容器中,不同温度及不同n(H2)/n(SiHCl3)时,反应物X的平衡转化率关系如图。下列判断合理的是
Si(s)+3HCl(g)。在2L密闭容器中,不同温度及不同n(H2)/n(SiHCl3)时,反应物X的平衡转化率关系如图。下列判断合理的是
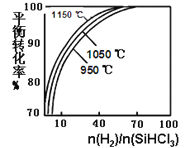
A. X是H2
B. 1150℃反应的平衡常数大于950℃时反应的平衡常数
C. 减小Si(s)的量,有利于提高SiHCl3的转化率
D. 工业上可采用增大压强的方法提高产率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是( )
A. 将Al条投入NaOH溶液中:Al+OH-+H2O===AlO![]() +H2↑
+H2↑
B. 氯气和水反应:Cl2+H2O === 2H++Cl-+ClO-
C. 碳酸氢钙溶液中加入过量的氢氧化钠溶液:HCO![]() +OH-===CO
+OH-===CO![]() +H2O
+H2O
D. 硫酸铵溶液和氢氧化钡溶液反应:Ba2++2OH-+2NH4++SO42-=BaSO4↓+2 NH3·H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过渡金属钛、铬、铁、镍、铜等金属及其化合物在工业上有用途。
(1)钛铁合金具有放氢温度低、价格适中等优点,是钛系储氢合金的代表。
①Ti的基态原子价电子排布式为_________。
②Fe元素在周期表中的位置是_________。
(2)制备 CrO2Cl2的反应为 K2Cr2O7+3CCl4=2KCl+2 CrO2Cl2+3COCl2↑。
①上述化学方程式中非金属元素电负性由小到大的顺序________。(用元素符号表示)
②COCl2分子中所有原子均满足8电子构型,COCl2分子中π键和σ键的个数比为____,中心原子的杂化方式为_______。
(3)NiO、FeO的晶体结构均与NaCl的晶体结构相似,其中Ni2+和Fe2+的离子半径分別为6.9×10-2nm和7.8×10-2nm。则熔点:FeO_____(填“>”“<”或“=” )NiO。
(4)Ni和La的合金是目前使用广泛的储氢材料,具有大容量、高寿命、耐低温等特点,在中国已实现了产业化.该合金的晶胞结构如图所示。

①该晶体的化学式为__________。
②已知该晶胞的摩尔质量为Mg/mol,密度为dg/cm3。设NA为阿伏加徳罗常数的值,则该晶胞的体积是_______(用含M、d、NA的代数式表示)。
③该晶体的内部具有空隙,且每个晶胞的空隙中储存6个氢原子比较温定。
已知:a=511pm,c=397pm;标准状况下氢气的密度为8. 98×10-5g/cm3;
![]() 。若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为________。
。若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pH=13的强碱溶液和pH=2的强酸溶液混合,所得溶液的pH=11,则强碱溶液和强酸溶液的体积之比为( )
A. 11:1 B. 9:1 C. 1:11 D. 1:9
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种短周期元素,原子序数依次增大。A、E同主族,且E元素原子的核外电子数是A元素原子核内质子数的两倍。B、C两元素原子的最外层电子数之和等于D元素原子的最外层电子数,C、D两元素原子最外层电子数之和等于F元素原子的最外层电子数。D元素原子最外层电子数是次外层电子数的一半。回答下列问题:
(1)用电子式表示B、F两元素形成化合物的过程:_______________________________。
(2)A、C两元素的化合物与B的氢氧化物反应的离子方程式为:___________________。
(3)B的最高价氧化物的水化物与C的最高价氧化物的水化物反应的离子方程式为:__________。
(4)写出下列物质的电子式,指出化学键类型。
B2E:___________、___________; EF2:___________、___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应A(g)+3B(g)![]() 2C(g)+2D(g) 在4种不同情况下反应速率分别如下,其中反应速率v最大的是
2C(g)+2D(g) 在4种不同情况下反应速率分别如下,其中反应速率v最大的是
A. v(A)=0.15mol/(L·min) B. v (B)=0.6 mol/(L·min)
C. v (C)=0.3 mol/(L·min) D. v (D)=0.1 mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2是硫元素重要的化合物,是大气主要污染物之一,是形成酸雨的主要原因,是以还原性为主的酸性氧化物,具有漂白性。
Ⅰ.检验SO2气体的实验方法和现象是______________。
Ⅱ.探究SO2气体的氧化性和还原性,可以使用的药品和装置如图1所示:

(1) 装置A中的现象是______,写出B中发生反应的离子方程式:______。
(2) 在上述装置中通入过量的SO2,为了验证B中SO2与Fe3+发生了氧化还原反应,取B中的溶液,分成两份,并设计了如下实验:
方案①:往第一份试液中加入少量酸性KMnO4溶液,紫红色褪去。
方案②:往第二份试液中加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
上述方案中不合理的是_________,原因是__________。
Ⅲ.使用如图2所示的装置进行实验,探究SO2与Na2O2的反应(图中铁架台等装置已略去)。

假设1 : 2SO2+2Na2O2=2Na2SO3+O2
假设2 : SO2+ Na2O2=2Na2SO4
(1) D装置的作用是______________。
(2)为验证假设1正确,需要进行的实验操作和现象是______________。
(3)为验证假设2正确,需要进行的实验操作和现象是______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com