
分析 (1)因为2SO2(g)+O2(g)?2SO3(g)+Q (Q>0)即放热反应,则升高温度,正反应速率增大,平衡向吸热方向移动;
(2)根据V=$\frac{△c}{△t}$进行计算.
解答 解:(1)因为2SO2(g)+O2(g)?2SO3(g)+Q (Q>0)即放热反应,则升高温度,正反应速率增大,平衡向吸热方向移动即逆方向移动,故答案为:增大;逆;
(2)由2SO2(g)+O2(g)?2SO3(g)反应,则20s后测得SO3的物质的量为0.08mol,则O2的变化量为0.04mol,所以O2的平均反应速率V=$\frac{△c}{△t}$=$\frac{\frac{0.04}{2}}{20}$=0.001mol/(L•s),故答案为:0.001.
点评 本题考查温度对化学平衡的影响以及反应速率的计算,注重了基础知识的考查,注意对基础知识的理解掌握,本题难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 元素 A、B 组成的化合物常温下一定呈气态 | |
| B. | 元素 D 的最高价氧化物对应的水化物不是两性化合物 | |
| C. | 元素 C 的最高价氧化物对应的水化物是弱碱 | |
| D. | 化合物 AE 与 CE 有相同类型的化学键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ①② | C. | ③④ | D. | ③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化剂 | B. | 还原剂 | ||
| C. | 既是氧化剂又是还原剂 | D. | 既不是氧化剂又不是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3+H2O→NH3•H2O | B. | H2+I2→2HI | ||
| C. | HClO→H++ClO- | D. | Cl2+2NaOH→NaCl+NaClO+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
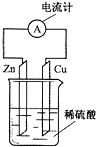
| A. | 锌片为正极,且锌片逐渐溶解 | B. | 铜片为负极,且铜片上有气泡 | ||
| C. | 溶液中的H+移向铜极 | D. | 该装置能将电能转变为化学能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2的比例模型: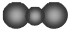 | |
| B. | 氢化铵(NH4H)电子式: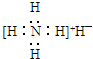 | |
| C. | (CH3)3COH的名称:2,2-二甲基乙醇 | |
| D. | 乙酸乙酯的水解CH3COOCH2CH3+H218O $?_{△}^{酸}$CH3CO18OH+CH3CH2OH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com