
分析 (1)铁与水蒸气在高温条件下反应生成四氧化三铁和氢气;Fe3O4粉可看做FeO•Fe2O3;
(2)KNO3、KOH、Fe2O3在加热共融,反应生成高铁酸钾、亚硝酸钾和水,根据得失电子相等、质量守恒配平;
(3)在充电时是电解池的工作原理,阳极上发生失电子的氧化反应,二价铅失去电子生成氧化铅.
解答 解:(1)铁与水蒸气在高温条件下反应生成四氧化三铁和氢气,反应方程式:3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2;
Fe3O4粉可看做FeO•Fe2O3,FeO中铁为+2价,Fe2O3中铁为+3价,所以产物中+2价的Fe和+3价Fe的物质量之比:1:2;
故答案为:3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2;1:2;
(2)KNO3、KOH、Fe2O3在加热共融,反应生成高铁酸钾、亚硝酸钾和水,K2FeO4中铁元素化合价为+6,则亚铁离子从+3价变为+6价,化合价升高3价,化合价至少升高3×2=6价;KNO3中N元素从+5降为KNO2中的+3价,化合价降低2价,则化合价最小公倍数为6,所以氧化铁的系数为1,KNO3的系数为3,然后根据质量守恒定律配平,配平后的方程式为:Fe2O3+3KNO3+4KOH=K2FeO4+3KNO2+2H2O,
故答案为:1 Fe2O3+3KNO3+4KOH=2K2FeO4+3KNO2+2H2O;
(3)充电时,阳极PbSO4发生氧化反应,电极反应为:PbSO4+2H2O-2e-=PbO2+4H++SO42-;
故答案为:PbSO4+2H2O-2e-=PbO2+SO42-+4H+.
点评 本题考查了氧化还原反应,主要涉及氧化还原反应方程式书写,准确分析反应中元素化合价变化及生成物判断是解题关键,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题
 .
. ,A与等物质的量的H2完全加成后,得到烃C,用系统命名法给C命名2-甲基丁烷.
,A与等物质的量的H2完全加成后,得到烃C,用系统命名法给C命名2-甲基丁烷.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 有机物(g) | 氢气(L) |
| 0.575 | 0.14 |
| 1.15 | 0.28 |
| 2.3 | 0.56 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molOH-离子中含电子数目为10NA | |
| B. | 0.5L 0.2mol•L-1的NaCl溶液中含有的Na+数是0.1NA | |
| C. | 分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量约为28 g | |
| D. | 1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molNa2O2固体中含阴离子个数为2NA | |
| B. | 1molSiO2中含Si-O的数目为2NA | |
| C. | 标准状况下,22.4L乙炔中含π键数为2NA | |
| D. | 1molNaHCO3晶体中阳离子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子数之比1:1 | B. | 密度之比4:11 | C. | 密度之比11:16 | D. | 体积之比11:16 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

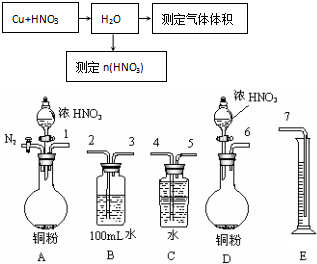
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
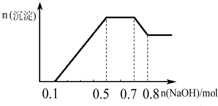
| A. | 溶液中的阳离子只有H+、Mg2+、Al3+ | |
| B. | 溶液中一定不含CO32-,一定含有SO42-和NO3- | |
| C. | 溶液中n(NH4+)=0.2 mol | |
| D. | 三种离子的物质的量之比n(H+):n(Al3+):n(Mg2+)=1:1:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com