
如图所示,甲、乙为相互串联的两电解池.
(1)甲池若为用电解原理精炼铜的装置,则A电极名称为阴极,电极材料是 ,电极反应式为 ,电解质溶液可以是 .
(2)乙池中Fe极电极反应式为 ,若在乙池中滴入少量酚酞试液,开始电解一段时间,Fe极附近呈 色.

考点: 原电池和电解池的工作原理.
专题: 电化学专题.
分析: (1)依据电解精炼的原理是粗铜做阳极,精铜做阴极,含铜离子的电解质溶液进行电解反应,在阴极是溶液中铜离子得到电子生成铜;
(2)乙池中Fe极为阴极,阴极阳离子放电,根据反应判断Fe附近的酸碱性.
解答: 解:(1)电解精炼的原理是粗铜做阳极,精铜做阴极,含铜离子的电解质溶液进行电解反应,在阴极是溶液中铜离子得到电子生成铜,电极反应是Cu2++2e﹣═Cu;
故答案为:阴;纯铜;Cu2++2e﹣═Cu;含铜离子的盐溶液;
(2)乙池C(石墨)极为电解池的阳极,Fe极为阴极,阴极阳离子放电,则Fe上氢离子得电子生成氢气,其电极反应为:2H++2e﹣═H2↑,同时Fe电极附近还生成氢氧根离子,所以加酚酞溶液变红色;
故答案为:2H++2e﹣═H2↑;红.
点评: 本题考查了电解原理的分析判断,装置分析判断电极名称是基础,掌握电化学基本知识是解题关键,题目难度不大.


 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:
下列方程式书写正确的是()
A. 碳酸的电离方程式:H2CO3⇌2H++CO32﹣
B. 向氯化钙溶液中通入二氧化硫气体:Ca2++SO2+H2O=CaSO3↓+2H+
C. 往AgI悬浊液中滴加Na2S饱和溶液:2Ag+ (aq)+S2﹣(aq)=Ag2S(s)
D. 明矾水解:Al3++3H2O⇌Al(OH)3+3H+
查看答案和解析>>
科目:高中化学 来源: 题型:
在同温同压下,下列各组热化学方程式中,Q2>Q1的是()
A. 2H2(g)+O2(g)=2H2O(g)△H=﹣Q1kJ/mol;
2H2(g)+O2(g)=2H2O(g))△H=﹣Q2kJ/mol
B. S(g)+O2(g)=SO2(g)△H=﹣Q1kJ/mol;
S(s)+O2(g)=SO2(g))△H=﹣Q2kJ/mol
C. C(s)+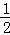 O2(g)=CO2(g))△H=﹣Q1kJ/mol;
O2(g)=CO2(g))△H=﹣Q1kJ/mol;
C(s)+O2(g)=CO(g))△H=﹣Q2kJ/mol
D. H2(g)+Cl2(g)=2HCl(g)△H=﹣Q1kJ/mol;
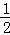 H2(g)+Cl2(g)=HCl(g))△H=﹣Q2kJ/mol
H2(g)+Cl2(g)=HCl(g))△H=﹣Q2kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
用惰性电极电解M(NO3)x的水溶液,当阴极上增重a g时,在阳极上同时产生b L氧气(标准状况),从而可知M的相对原子质量为()
A.  B.
B.  C.
C.  D.
D. 
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生设计了一个“黑笔写红字”的趣味实验.滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹.据此,下列叙述正确的是()

A. 铅笔端作阳极,发生还原反应
B. 铂片端作阴极,发生氧化反应
C. 铅笔端有少量的氯气产生
D. a点是负极,b点是正极
查看答案和解析>>
科目:高中化学 来源: 题型:
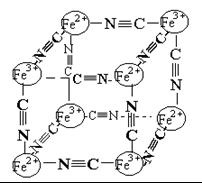
分析化学中常用X射线研究晶体结构,有一种蓝色晶体可表示为:MxFey(CN)z,研究表明它的结构特性是Fe2+、Fe3+分别占据立方体的顶点,自身互不相邻,而CN一位于立方体的棱上,其晶体中的阴离子结构如图示,下列说法正确的是( )
A.该晶体是原子晶体
B.M的离子位于上述立方体的面心,呈+2价
C.M的离子位于上述立方体的体心,呈+1价,且M+空缺率(体心中没有M+的占总体心的百分比)为50%
D.晶体的化学式可表示为MFe2(CN)3,且M为+1价
查看答案和解析>>
科目:高中化学 来源: 题型:
天然气(主要成分甲烷)含有少量含硫化合物[硫化氢、羰基硫(COS)、乙硫醇(C2H5SH)],可以用氢氧化钠溶液洗涤除去。
(1)硫元素的原子结构示意图为 ;羰基硫分子的电子式为 。
(2)下列说法正确的是 。
a. 乙硫醇的相对分子质量大于乙醇,故其沸点更高
b. 同温度同浓度下Na2CO3溶液的pH大于Na2SO4溶液,说明硫元素非金属性强于碳元素
c. H2S分子和CO2都是极性分子,因为它们都是直线形分子
d. 由于乙基的影响,乙硫醇的酸性弱于H2S
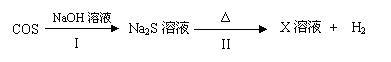 (3)羰基硫用氢氧化钠溶液处理及利用的过程如下(部分产物已略去):
(3)羰基硫用氢氧化钠溶液处理及利用的过程如下(部分产物已略去):
①反应I除生成两种正盐外,还有水生成,其化学方程式为 。
②已知X溶液中硫元素的主要存在形式为S2O32-,则II中主要反应的离子方程式为 。
③右图是反应II中,在不同反应温度下,反应时间与H2产量的关系图
(Na2S初始含量为3 mmo1)。
a. 判断T1、T2、T3的大小: ;
b. 在T1温度下,充分反应后,若X溶液中除S2O32-外,还有因发生副反应而同时产生的SO42-,则溶液中c(S2O32-):c(SO42-)= 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com