
| A.使用吸收塔设备 | B.使用加压条件 |
| C.使用氢气做原料 | D.使用催化剂 |
科目:高中化学 来源:不详 题型:问答题
| A.增大空气的进入量,或减少天然气进入量 |
| B.增大空气的进入量,也增大天然气进入量 |
| C.减少空气的进入量,或增大天然气进入量 |
| D.减少空气的进入量,也减少天然气进入量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.合成氨工业是将氮气和氢气在铁催化剂的表面转化成氨气 |
| B.在燃料电池中,氢气和氧化剂在催化剂表面反应所产生的能量转化为电能 |
| C.汽车中装有催化器,能将尾气中一氧化碳和氮氧化物转化为二氧化碳和氮气 |
| D.加酶洗衣粉的乳化作用能将衣物纤维表面的油渍洗去 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.此法的优点之一是原料取自大海 |
| B.进行①②③步骤的目的是富集MgCl2 |
| C.可用电解熔融氧化镁的方法制取镁 |
| D.电解法冶炼金属要消耗大量的电能 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
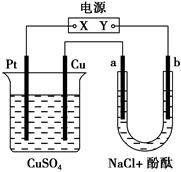
| A.X是正极,Y是负极 |
| B.X是负极,Y是正极 |
| C.CuSO4溶液的pH逐渐变小 |
| D.CuSO4溶液的pH不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.离子交换法 | B.中和法 | C.反渗透法 | D.蒸馏法 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.海水中蕴含的元素有80多种,其中Mg、Br、I在海水中的总储量分别约为1.8×1015t、1×1014t、8×1010t。由于海水中镁的储量很大,工业上常以海水为原料提取镁,因此,镁元素被称为“海洋元素” |
B.对于可逆反应N2(g)+3H2(g)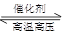 2NH3(g),增大氮气浓度可增加活化分子百分数,从而使反应速率增大 2NH3(g),增大氮气浓度可增加活化分子百分数,从而使反应速率增大 |
| C.硫酸工业中,从吸收塔上部导出的气体再次通入接触室进行二次氧化,进一步吸收后,二氧化硫的含量很少,可直接排放到空气中 |
| D.阴极射线和α-粒子散射现象都对原子结构模型的建立做出了贡献 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
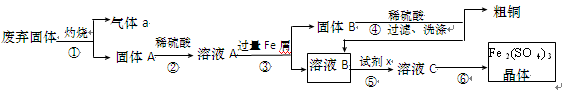
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com