
| A. | MnO2 | B. | KMnO4 | C. | NaClO | D. | KClO3 |
分析 题中四种物质与盐酸反应都可生成氯气,反应中盐酸表现为还原性和酸性,结合反应的方程式判断.
解答 解:设都生成1molCl2,
A.发生MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,生成1molCl2消耗4molHCl;
B.发生2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O,生成1molCl2消耗3.2molHCl;
C.发生NaClO+2HCl=NaCl+Cl2↑+H2O,生成1molCl2消耗2molHCl;
D.发生KClO3+6HCl=KCl+3Cl2↑+3H2O,生成1molCl2消耗2molHCl;
则消耗盐酸最多的为MnO2,
故选A.
点评 本题考查氧化还原反应,为高频考点,侧重分析与计算能力的考查,注意把握反应的相关化学方程式的书写,题目难度不大.


 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②③④⑤ | C. | ①③④⑤ | D. | ⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
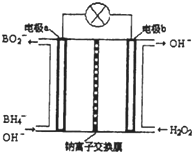 硼氢化钠(NaBH4)是有机合成中的重要还原剂,最新研究发现,以NaBH4和H2O2为原料,NaOH溶液作电解质溶液,可以设计成全液流电池,其工作原理如图所示,假设电池工作前左右两槽溶液的体积各为1L,回答下列问题:
硼氢化钠(NaBH4)是有机合成中的重要还原剂,最新研究发现,以NaBH4和H2O2为原料,NaOH溶液作电解质溶液,可以设计成全液流电池,其工作原理如图所示,假设电池工作前左右两槽溶液的体积各为1L,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X>2 | B. | X=2 | C. | 2>X>1 | D. | X=1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu2++2OH-═Cu(OH)2↓ CuCO3+2NaOH═Cu(OH)2↓+Na2CO3 | |
| B. | CO32-+2H+═H2O+CO2↑ BaCO3+2HCl═BaCl2+H2O+CO2↑ | |
| C. | Ca2++CO32-═CaCO3↓ Ca(OH)2+K2CO3═CaCO3↓+2KOH | |
| D. | H++OH-═H2O Ba(OH)2+H2SO4═BaSO4+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com