
| A. | 戊醇 | B. | 戊烷 | ||
| C. | 戊烯 | D. | 戊醛(C5H10O,仅含一个-CHO) |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 1.5mol单质Fe粉在足量氧气中完全燃烧,失去4NA个电子 | |
| B. | 在25g质量分数为60%的乙酸水溶液中,含有氢原子数为NA | |
| C. | 7.8 gNa2S和Na2O2 的混合物中,含有的阴离子数等于0.15NA | |
| D. | 在5×107Pa、500°C和铁触媒作用下,1molN2和3molH2可生成氨气分子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
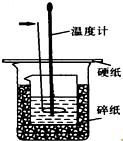 50ml0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中放出的热量可计算中和热.回答下列问题:
50ml0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中放出的热量可计算中和热.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH2OH | B. | COOH-CHOH-CHCl-COOH | ||
| C. | CFCl3 | D. | CH2OH-CHOH-CH2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
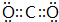 .D2A2中所含化学键类型为非极性共价键和离子键.
.D2A2中所含化学键类型为非极性共价键和离子键. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
. ;
;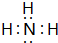 ,G的结构式为
,G的结构式为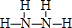 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸钠的电离方程式:Na2SO4=Na2++SO42- | |
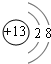
| B. | Mg2+的结构示意图: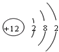 | |
| C. | 氮气的结构式::N≡N: | |
| D. | 氯化镁的电子式: |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com