
| A����̼��Ũ���Ṳ�ȷ�Ӧ�����������ͨ���������������Һ��CO2+SO2+3OH-=HSO3-+CO32-+H2O |
| B����Ca��ClO��2��Һ��ͨ��������� Ca2++2ClO-+SO2+H2O=2HClO+CaSO3�� |
| C����Fe��NO3��3��Һ�м��������HI��Һ 2NO3-+8H++6I-=3I2+2NO��+4H2O |
| D��������������ʵ���Ũ�ȵ�NaHCO3��Һ��Ba��OH��2��Һ���HCO3-+Ba2++OH-=BaCO3��+H2O |
| ||


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����λʱ��������amolA2��ͬʱ����2amolAB |
| B�������е���ѹ����ʱ����仯 |
| C��A2��B2��ABŨ�Ȳ���ʱ����仯 |
| D��v��A2����v��B2����v��AB��=1��1��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���Ȼ��ƵĻ�ѧʽ CaCl |
B��þ���ӽṹʾ��ͼ��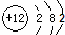 |
| C��̼���Ƶĵ��뷽��ʽ Na2CO3=Na++CO32- |
| D�����������ĵ��뷽��ʽBa��OH��2=Ba2++2OH- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1mol O |
| B��1mol O2 |
| C��1mol������ |
| D��1Ħ��ƻ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ͬ�����£�N2��O3�Ļ��������������N2����ԭ������� |
| B�������ʵ����ļ���-CH3�����ǻ���-OH��������������� |
| C�����³�ѹ��28 g CO��22.4 L O2������������� |
| D��16 g CH4��18 g NH������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���������е�����������Һ�������е���Ԫ�أ�Ag++Br-=AgBr�� | ||||
| B��14g��ϩȼ������Һ̬ˮ����b kJ���������ʾ��ȼ���ȵ��Ȼ�ѧ����ʽΪ��C2H4��g��+3 O2��g���T2 H2O��g��+2 CO2��g����H=-2 b kJ?mol-1 | ||||
C���ö��Ե缫��ⱥ��KCl��Һ��2 H++2 Cl-
| ||||
| D������������˫��ˮ��ϡH2SO4��ϣ�2 Fe2++H2O2+2 H+=2 Fe3++2 H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
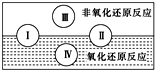 ����֪ˮ���������Ҫ��ɲ��֣��������к�������һ�����ʣ��������ֻ�����Ӧ������������ԭ��Ӧ�Ĺ�ϵ��Ҳ������ͼ�����д����ˮ�μӵķ��Ϸ�Ӧ���͢���һ����ѧ����ʽ��
����֪ˮ���������Ҫ��ɲ��֣��������к�������һ�����ʣ��������ֻ�����Ӧ������������ԭ��Ӧ�Ĺ�ϵ��Ҳ������ͼ�����д����ˮ�μӵķ��Ϸ�Ӧ���͢���һ����ѧ����ʽ��
| ||
4- 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ϡ�����м���ͭ�ۣ�ͭ�۲��ܽ⣻�ټ���K NO3 ���壬ͭ���Բ��ܽ� |
| B���������ʵ���Cl2��SO2ͨ��Ʒ����Һ��Ư������ǿ |
| C��ŨH2SO4��Cu��C��Ӧ������ȣ�Ũ������Cu��C��Ӧ��������� |
| D��������������С�մ���臨���������������������������Һ��Ӧ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com