
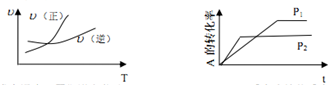
| A. | 升高温度,平衡逆向移动 | B. | m<p,正反应为放热反应 | ||
| C. | m+n<p,正反应为吸热反应 | D. | 减小压强,平衡逆向移动 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | I-和IO-都是该反应的催化剂 | |
| B. | H2O2分解的速率取决于第二步反应的快慢 | |
| C. | 反应物的总能量比生成物总能量低98kJ | |
| D. | 第一步H2O2被还原,第二步H2O2被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溴乙烷通常是由溴跟乙烷直接反应来制取 | |
| B. | 在溴乙烷中滴入硝酸银,立即析出浅黄色沉淀 | |
| C. | 溴乙烷跟KOH的醇溶液加热反应生成乙醇 | |
| D. | 溴乙烷不溶于水,溶于有机溶剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业生产中常用静电除尘装置除去废气中的固体悬浮物 | |
| B. | 三氯化铁溶液中滴入氢氧化钠溶液出现红褐色沉淀 | |
| C. | 一束平行光线照射豆浆时,可看到光亮的通路 | |
| D. | 万里长江流入大海处,形成长江三角洲 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 做金属锂与水反应实验时,用镊子取出锂后要用滤纸吸干煤油 | |
| B. | 实验时制氢气,为了加快反应速率,可向稀H2SO4中滴加少量Cu(NO3)2溶液 | |
| C. | 排出碱式滴定管尖嘴端气泡的操作是向上弯曲橡皮管,然后挤压玻璃球 | |
| D. | 实验室配制500mL0.2mol•L-1NaCl溶液,需用托盘天平称量5.85gNaCl固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 金属离子 | Fe2+ | Fe3+ | Al3- | Mg2+ | Ni2+ |
| 开始沉淀的pH值 | 6.5 | 1.6 | 3.4 | 9.4 | 7.2 |
| 完全沉淀的pH值 | 9.7 | 3.2 | 5.4 | 12.4 | 9.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤的气化和液化是使煤变成清洁能源的有效途径 | |
| B. | 煤的干馏过程属于物理变化,通过干馏可以得到焦炉气、煤焦油、焦炭等产品 | |
| C. | 工业上大量燃烧含硫燃料是形成“酸雨”的主要原因 | |
| D. | 以煤为原料可获得许多合成高分子材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ,结构简式H2C=CH2.
,结构简式H2C=CH2.
 ,反应类型是加聚反应.
,反应类型是加聚反应.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com