
【题目】(1)在苯酚钠溶液中通入少量的CO2,写出反应的化学方程式:_______________;
(2)丙酸与乙醇发生酯化反应的的化学方程式:_______________;
(3)1,2—二溴丙烷发生消去反应:_______________;
(4)甲醛和新制的银氨溶液反应:_______________。
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W四种短周期元素在元素周期表中的相对位置如图所示。其中元素Z的基态原子价电子层排布为nsn-1npn+1,下列说法正确的是
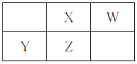
A.Y、Z、W三种元素的最高正价依次递增
B.X、Z都是第ⅥA族元素,电负性:W>X>Z
C.氢化物稳定性Z>Y>W
D.对应的简单离子半径:W>X>Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将![]() 转变为
转变为![]() 的方法为( )
的方法为( )
A.溶液加热,通入足量的HCl
B.与足量的NaOH溶液共热后,再通入CO2
C.与稀H2SO4共热后,加入足量的Na2CO3
D.与稀H2SO4共热后,加入足量的NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下面的合成路线图完成下面小题

【1】化合物D的名称为( )
A.乙醇B.乙烷C.葡萄糖D.乙酸
【2】乳酸的一种合成方法如图所示,下列说法正确的是( )
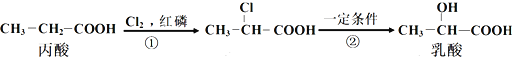
A.步骤①、②分别是加成反应、取代反应
B.蛋白质水解也可生成乳酸
C.丙酸烃基上的二氯代物有2种
D.乳酸与丙烯完全燃烧的产物相同
【3】有下列三种有机物,实现它们之间相互转化所选试剂(均足量)正确的是____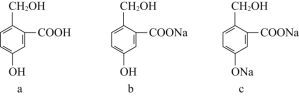
a转化为b | a转化为c | c转化为b | |
A | NaOH | Na | CO2 |
B | Na2CO3 | NaOH | HCl |
C | NaHCO3 | NaOH | CO2 |
D | NaHCO3 | Na2CO3 | HCl |
A.AB.BC.CD.D
【4】化合物A(C4H8Br2)可由下列反应制得,C4H10O![]() C4H8
C4H8![]() C4H8Br2,则A的结构式不可能的是( )
C4H8Br2,则A的结构式不可能的是( )
A.![]() B.
B.![]()
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
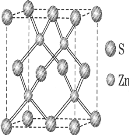
【题目】有A、B、C、D、E、F六种元素,A是周期表中原子半径最小的元素,B是电负性最大的元素,C的2p轨道中有三个未成对的单电子,F原子核外电子数是B与C核外电子数之和,D是主族元素且与E同周期,E能形成红色(或砖红色)的E2O和黑色的EO两种氧化物,D与B可形成离子化合物,其晶胞结构如图所示.请回答下列问题.
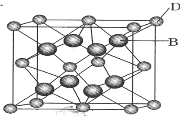
(1)E元素原子基态时的电子排布式为_________.
(2)A2F分子中F原子的杂化类型是_________
(3)CA3极易溶于水,其原因主要是_________,
(4)富勒烯衍生物由于具有良好的光电性能,在太阳能电池的应用上具有非常光明的前途.富勒烯(C60)的结构如图,分子中碳原子轨道的杂化类型为_________;1molC60分子中σ键的数目为_________.

(5)多元化合物薄膜太阳能电池材料为无机盐,其主要包括砷化镓、硫化镉、硫化锌及铜铟硒薄膜电池等.
①第一电离能:As_________Se(填“>”“<”或“=”).
②硫化锌的晶胞中(结构如图所示),硫离子的配位数是_________与S距离最近且等距离的S之间的距离为_________(密度为ρg/cm3)
③二氧化硒分子的空间构型为_________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】迷迭香酸是从蜂花属植物中提取得到的酸性物质,其结构如图.下列叙述正确的是( )
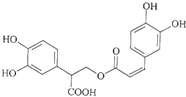
A.迷迭香酸可以发生水解反应、取代反应和酯化反应
B.1mol迷迭香酸最多能和8mol氢气发生加成反应
C.1mol迷迭香酸与NaOH的水溶液完全反应时最多消耗5molNaOH
D.迷迭香酸属于芳香烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W、Q在元素周期表中的位置如表所示。下列说法不正确的是( )
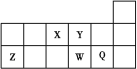
A.元素X与元素Z的最高正化合价之和的数值等于8
B.Y2-和Z3+具有相同的电子层结构
C.原子半径的大小顺序为rQ>rW>rZ>rY>rX
D.元素W的最高价氧化物对应水化物的酸性比Q的弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】足量铜与一定量的浓硝酸反应,得到硝酸铜溶液和NO2、NO的混合气体2.24L(标准状况),这些气体与一定体积O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入4 mol/LNaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是50 mL,下列说法正确的是 ( )
A. 混合气体中含NO21.12 L B. 消耗氧气的体积为1.68 L
C. 此反应过程中转移的电子为0.3 mol D. 参加反应的硝酸是0.4mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下图所示装置回答以下问题。已知:①KMnO4常温下与浓盐酸反应可制得Cl2。②H2SiO3不溶于水。
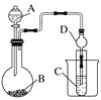
(1)利用如图装置可以验证元素非金属性的变化规律。图中A装置的名称是________________。干燥管D的作用是____________。
(2)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性强于硫:烧瓶中发生反应的离子方程式为____________________________。装置C中的实验现象为有淡黄色沉淀生成,离子方程式为_____________________。
(3)若要用此装置证明酸性:HNO3>H2CO3>H2SiO3,进而证明非金属性:N>C>Si,从以下所给物质中选出甲同学设计的实验所用到的物质:①稀HNO3 ②稀盐酸 ③碳酸钙 ④Na2SiO3溶液 ⑤SiO2。试剂A与C分别为________(填序号);试管中发生反应的离子方程式为__________________。有同学认为此实验不能说明N、C、Si的非金属性强弱,你认为原因是_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com