
【题目】下列关于有机物的叙述正确的是
A. 酸性高锰酸钾溶液可以检验出苯和乙醇的混合液中的乙醇
B. 与NaOH溶液反应且分子式为C2H4O2的有机物一定是乙酸
C. 丙烯分子中可能有8个原子共处于同一平面
D. 甲苯的一氯代物有3种
科目:高中化学 来源: 题型:
【题目】下列分子中的中心原子杂化轨道的类型相同的是( )
A. CO2与SO2 B. CH4与NH3 C. BeCl2与BF3 D. C2H2与C2H4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~E都是有机化合物,A为一取代芳香烃,B中含有一个甲基。它们的转化关系如下:

(1)由A生成B、由D生成E的反应类型分别是__________、__________;
(2)由B生成C的化学方程式为__________;
(3)由B生成D的反应条件是__________;
(4)A的名称为__________;E的官能团名称为__________;
(5)在E的同分异构体中,苯环上一硝化的产物只有一种,其中核磁共振氢谱有两组峰,且峰面积比为1:1的是__________(写结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】3,5-二甲氧基苯酚是重要的有机合成中间体,可用于天然物质白柠檬素的合成。一种以间苯三酚为原料的合成反应如下:( )

物质 | 沸点/℃ | 熔点/℃ | 溶解性 |
甲醇 | 64. 7 | ﹣97.8 | 易溶于水 |
3,5-二甲氧基苯酚 | 172~175 | 33~36 | 易溶于甲醇、乙醚,微溶于水 |
下列说法正确的是( )
A. 分离出甲醇的操作是结晶 B. 间苯三酚与苯酚互为同系物
C. 上述合成反应属于取代反应 D. 洗涤时可以用饱和Na2CO3溶液除氯化氢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇(CH3OH)是重要的溶剂和替代燃料,工业常以CO和H2的混合气体为原料一定条件下制备甲醇
(1)甲醇与乙醇互为_______________;完全燃烧时,甲醇与同物质的量的汽油(设平均组成为C8H18)消耗O2量之比为________________。
(2)工业上常用“水煤气法”获得CO和H2其反应原理如下:
C(s)+H2O(g)![]() CO(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2(g) CO(g)+H2O(g)![]() CO2(g)+H2(g)
CO2(g)+H2(g)
某水煤气样品中含0.2LCO、0.5LCO2,则该样品中含H2_________L。
(3)工业上还可以通过下列途径获得H2,其中节能效果最好的是_______________。
a.高温分解水制取H2:2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
b.电解水制取 H2:2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
c.甲烷与水反应制取H2:CH4+H2O![]() 3H2+CO
3H2+CO
d.在光催化剂作用下,利用太阳能分解水制取H2:2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
(4)在2L的密闭容器中充入lmoCO和2molH2,—定条件下发生反应:
CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
测得CO和CH3OH(g)浓度变化如图所示。

①从反应开始到平衡,氢气的平均反应速率v(H2)=_____mol·L-1·min-1。
②能够判断该反应达到平衡的是_________填选项)。
a.CO、H2和CH3OH三种物质的浓度相等
b.密闭容器中混合气体的密度不再改变
c.CH3OH分解的速率和CH3OH生成的速率相等
d.相同时间内消耗lmolCO,同时消耗1molCH3OH
(5)为使合成甲醇原料的原子利用率达100%,实际生产中制备水煤气时还使用CH4,则生产投料时,n(C):n(H2O):n(CH4)=____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示装置Ⅰ是—种可充电电池,离子交换膜只允许Na+通过,电池充放电的化学方程式为2Na2S2+ NaBr3![]() 3NaBr+Na2S4;装置Ⅱ为电解池,闭合开关K时,b极附近先变红色。下列说法正确的是
3NaBr+Na2S4;装置Ⅱ为电解池,闭合开关K时,b极附近先变红色。下列说法正确的是

A. 放电时,电极A的反应式为:2S22--2e-=S42-
B. 放电时,正极的反应式为:Br3- +2e-=3Br-
C. 装置Ⅰ放电时,Na+的移动方向为电极A→电极B
D. 装置Ⅱ若将a、b的铜棒、铅笔芯互换,反应现象仍然相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼及其化合物在材料制造、有机合成等方面用途非常广泛。回答下列问题:
(1)VB2是一种导电陶瓷材料,基态钒原子的价电子排布图为_______。
(2)B、C、N三种元素第一电离能由小到大的顺序为________。
(3)硼的卤化物在工业中有重要作用,硼的四种卤化物的沸点如下表所示。
BF3 | BCl3 | BBr3 | BI3 | |
沸点/K | 172 | 285 | 364 | 483 |
①四种卤化物沸点依次升高的原因是__________________。
②用BF3分子结构解释反应BF3(g)+NH4F(s)==NH4[BF4] (s)能够发生的原因:____________。
制备环硼氨烷的方法如下:
![]()
BCl3、LiBH4中硼原子的杂化轨道类型依次为_________;与B3N3H6互为等电子体的分子的结构简式为________________。
(4)立方氮化硼的熔点为3000℃,其晶胞结构如图所示,晶胞参数a=361.5pm。
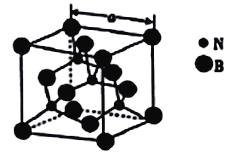
①立方氮化硼的晶体类型为_______________。
②紧邻的两个硼原子间的距离为_______(列出计算式即可) pm。
③立方氮化硼的密度为_____(列出计算式即可)g㎝-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】紫菜与海带类似,是一种富含生物碘的海洋植物,商品紫菜轻薄松脆、比海带更易被焙烧成灰(此时碘转化为碘化物无机盐),用于碘单质的提取,己知:
乙酵 | 四氯化碳 | 裂化汽油 | 碘(晶体) | |
密度gcm-3 | 0.7893 | 1.595 | 0.71~0.76 | 4.94 |
沸点/℃ | 78.5 | 76.8 | 25~232 | 184.35 |
以下为某兴趣小组模拟从紫菜提取碘单质的过程:
![]()
(1)实验室焙烧紫菜,需要下列仪器中的___________(填序号)。
a.试管 b.烧杯 c.坩埚 d.泥三角 e.蒸发皿 f.酒精灯 g.燃烧匙
(2)将焙烧所得的紫菜灰与足量的双氧水和稀硫酸作用,写出反应的离子方程式___________。
(3)操作①的名称是__________;试剂A为_________ (填本题表格中一种最佳化学试剂的名称),不使用另外两种试剂的主要原因分别是:I_____________________;II __________________。
(4)操作②应在____________(仪器名称)中振荡、静置;观察到的现象是______________。
(5)该方案采用常压加热蒸馏并不合理,理由是____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com