
【题目】CH4和H2O(g)可发生催化重整反应:CH4(g)+H2O(g)![]() CO(g)+3H2(g)。
CO(g)+3H2(g)。
(1)每消耗8g CH4转移的电子的数目为________________。
(2)已知:①2CO(g)+O2(g)=2CO2(g) △H1=akJ·mol-1
②CO(g)+H2O(g)=CO2(g)+H2(g)△H2=bkJ·mol-1
③CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H3=ckJ·mol-1
④CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H4
CO(g)+3H2(g) △H4
由此计算△H4=_____________kJ·mol-1。
(3)T℃时,向1L恒容密闭容器中投入1molCH4和1molH2O(g),发生反应:CH4(g)+H2O(g)![]() CO(g)+3H2(g),经过tmin,反应达到平衡。已知平衡时,c(CH4)=0.5mol·L-1。
CO(g)+3H2(g),经过tmin,反应达到平衡。已知平衡时,c(CH4)=0.5mol·L-1。
①0~tmin内,该反应的平均反应速率v(H2)=___________。
②T℃时,该反应的甲烷的转化率是_________。
③下列表述能作为反应达到化学平衡状态的标志是_____________。
a.反应速率v(CH4):v(H2) =1:3 b.各组分的物质的量浓度不再改变
c.混合气体的平均相对分子质量不再改变 d.混合气体的密度不变
e.单位时间内生成n molH2O的同时,生成3n mol H2 f.单位时间内4mol C—H键断裂的同时2mol O—H键也断裂
【答案】3NAc+3b-2a![]() mol·L-1·min·-10.5bce;
mol·L-1·min·-10.5bce;
【解析】
(1)消耗8gCH4转移电子物质的量为![]() mol=3mol,即转移电子个数为3NA;(2)根据盖斯定律,依据目标反应方程式应得出:③+3×②-2×①,即△H=(c+3b-2a)kJ·mol-1;(3)CH4(g)+H2O(g)
mol=3mol,即转移电子个数为3NA;(2)根据盖斯定律,依据目标反应方程式应得出:③+3×②-2×①,即△H=(c+3b-2a)kJ·mol-1;(3)CH4(g)+H2O(g)![]() CO(g)+3H2(g)
CO(g)+3H2(g)
起始:1 1 0 0
变化:0.5 0.5 0.5 1.5
平衡:0.5 0.5 0.5 1.5 根据化学反应速率的数学表达式,v(H2)= ![]() mol/(L·min)=
mol/(L·min)= ![]() mol/(L·min);②甲烷的转化率为0.5/1×100%=50%或甲烷的转化率为0.5;③a、没有指明速率的方向,故a错误;b、根据化学平衡状态的定义,各组分物质的量浓度不再改变,说明反应达到平衡,故b正确;c、根据M=m/n,组分都是气体,则气体质量不变,向正反应方向进行,气体物质的量增大,因此当M不再改变,说明反应达到平衡,故c正确;d、根据ρ=m/V,组分都是气体,则气体质量保持不变,容器为恒容状态,因此密度不变,不能说明反应达到平衡,故d错误;e、生成nmolH2O,反应向逆反应方向进行,生成3nmolH2,反应向正反应方向进行,且两者物质的量之比等于系数之比,故e正确;f、断裂C-H键和断裂O-H键反应都是向正反应方向进行,故f错误。
mol/(L·min);②甲烷的转化率为0.5/1×100%=50%或甲烷的转化率为0.5;③a、没有指明速率的方向,故a错误;b、根据化学平衡状态的定义,各组分物质的量浓度不再改变,说明反应达到平衡,故b正确;c、根据M=m/n,组分都是气体,则气体质量不变,向正反应方向进行,气体物质的量增大,因此当M不再改变,说明反应达到平衡,故c正确;d、根据ρ=m/V,组分都是气体,则气体质量保持不变,容器为恒容状态,因此密度不变,不能说明反应达到平衡,故d错误;e、生成nmolH2O,反应向逆反应方向进行,生成3nmolH2,反应向正反应方向进行,且两者物质的量之比等于系数之比,故e正确;f、断裂C-H键和断裂O-H键反应都是向正反应方向进行,故f错误。


科目:高中化学 来源: 题型:
【题目】某小组为研究电化学原理,设计如图装置,下列叙述不正确的是

A. a和b不连接时,铁片上会有金属铜析出
B. a和b用导线连接时,铁片上发生的反应为: Fe2e===Fe2+
C. a和b用导线连接时,电子从Cu片流向铁片
D. a和b用导线连接时,Cu2+向铜电极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁及其化合物一般无毒(或低毒)、无污染,镁电池放电时电压高且平稳,因此镁电池越来越成为人们研制绿色电池的焦点。其中一种镁电池的反应:为:xMg+Mo3S4![]() MgxMo3S4;在镁原电池放电时,下列说法错误的是( )
MgxMo3S4;在镁原电池放电时,下列说法错误的是( )
A. Mg2+向正极迁移 B. 正极反应为:Mo3S4+2xe-═Mo3S42x-
C. Mo3S4发生氧化反应 D. 负极反应为:xMg-2xe-═xMg2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4A(g)+ 5B(g)== 4C(g)+ 6D(g)在10L的密闭容器中进行,半分钟后,D的物质的量增加了0.45mol,则此反应的平均速率v(x)可表示为( )
A. v(A)=0.0010mol·L-1·s-1
B. v(B)=0.0010mol·L-1·s-1
C. v(C)=0.010mol·L-1·s-1
D. v(D)=0.045mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将0.1mol/L的一元酸HA溶液逐滴滴加到10mL0.1mol/LNaOH溶液中,pH的变化曲线如图所示。下列说法错误的是

A. a点所示溶液中c(Na+)>c(A-)>c(OH-)>c(HA)
B. a、b两点所示溶液中水的电离程度a点大于b点
C. pH=7时,c(Na+)=c(A-)+c(HA)
D. 一元酸HA为弱酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随原子序数递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如图所示。
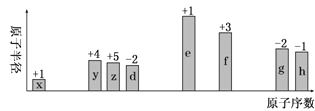
根据判断出的元素回答问题:
(1)z在周期表中的位置是_________________________________。
(2)写出x和d组成的一种四原子共价化合物的电子式_______________。
(3)y、g、h的最高价氧化物对应水化物的酸性最强的是______________(填化学式)。
(4)写出f的最高价氧化物与e的最高价氧化物对应的水化物反应的离子方程式______。
(5)已知e和g的最高价氧化物对应的水化物的稀溶液反应生成1mol水时所放出的热量为Q kJ。请写出该反应的中和热的热化学方程式___________。
(6)用y元素的单质与f元素的单质可以制成电极浸入由x、d、e三种元素组成的化合物的溶液中构成电池负极反应式为___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是某药物中间体的结构示意图:

试回答下列问题:
⑴观察上面的结构式与立体模型,通过对比指出结构式中的“Et”表示_______________;该药物中间体分子的化学式为_____________。
⑵解决有机分子结构问题的最强有力手段是核磁共振氢谱(PMR)。有机化合物分子中有几种化学环境不同的氢原子,在PMR中就有几个不同的吸收峰,吸收峰的面积与H原子数目成正比。
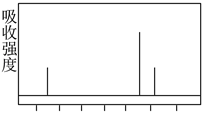
现有一种芳香族化合物与该药物中间体互为同分异构体,其模拟的核磁共振氢谱图如上图所示,试写出该化合物的结构简式:_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com