
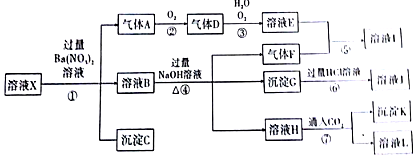
分析 某强酸性溶液X,则溶液中不存在弱酸根离子CO32-、SiO32-,溶液和硝酸钡溶液反应生成沉淀C,则溶液呈存在SO42-,不存在和硫酸根离子反应的Ba2+,C是BaSO4;
酸性条件下硝酸根离子具有强氧化性,所以溶液中Fe2+和NO3-不能共存,加入硝酸钡产生气体,则溶液中存在Fe2+,不存在NO3-,A是NO;
溶液B中加入氢氧化钠溶液时,产生气体F,则溶液中含有NH4+,F是NH3,产生沉淀,则溶液中存在Fe3+,沉淀G是Fe(OH)3,氢氧化铁和盐酸反应生成FeCl3,则J是FeCl3,溶液H中通入过量二氧化碳生成沉淀,则溶液中存在Al3+,沉淀K是Al(OH)3,溶液L是NaHCO3;
A是NO,则D是NO2,二氧化氮化和水反应生成硝酸和NO,则E是HNO3,硝酸和氨气反应生成硝酸铵,则I是NH4NO3,以此解答该题.
解答 解:(1)由强酸性条件即可判断溶液X中一定不存在弱酸根离子,所以不存在的离子有CO32-、SiO32-,
故答案为:CO32-、SiO32-;
(2)A.由以上分析不能确定是否存在Al3+,故A错误;
B.氨气被氧化只生成NO,故B错误;
C.由以上分析可知沉淀C一定是BaSO4、沉淀G一定是Fe(OH)3、沉淀K可能有Al(OH)3,故C正确;
D.溶液X中,含有亚铁离子,则一定没有NO3-,故D正确,
故答案为:CD;
(3)亚铁离子和硝酸反应生成铁离子、一氧化氮和水,离子反应方程式为:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,
故答案为:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O;
(4)氢氧化铁和稀盐酸反应生成氯化铁和水,氢氧化铁为红褐色沉淀,氯化铁溶液呈黄色,所以看到的现象是:红褐色沉淀逐渐溶解,溶液变为黄色,
故答案为:红褐色沉淀溶解,溶液变为黄色;
(5)转化的方程式为4NO2+O2+2H2O=4HNO3,氧化剂与还原剂的物质的量之比为1:4,故答案为:1:4;
(6)溶液中存在Fe2+,可被氧化生成Fe3+,则不能确定原溶液是否含有Fe3+,可加KSCN溶液检验,做法是取少量X溶液于试管中,加入几滴KSCN溶液,溶液不变红色说明无Fe3+,向溶液中逐滴加入NaOH溶液,有沉淀生成,持续滴加过量NaOH,沉淀减小但不消失则有Al3+.
故答案为:可以另取X溶液,先加入KSCN溶液,若溶液变为血红色则有Fe3+,再向溶液中逐滴加入NaOH溶液,有沉淀生成,持续滴加过量NaOH,沉淀减小但不消失则有Al3+.
点评 本题考查无机物的推断,根据物质间发生反应的特殊现象结合离子共存来分析解答,熟悉物质的性质是解本题关键,根据溶液和硝酸钡反应生成气体确定溶液中存在亚铁离子,为解答本题的易错点,熟练掌握离子共存的条件,灵活运用知识解答,题目难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同温同压下,气体的物质的量与体积成反比 | |
| B. | 同温同体积时,气体的物质的量与压强成反比 | |
| C. | 同温同物质的量时,气体的压强与体积成正比 | |
| D. | 同压同体积时,气体的物质的量与温度成反比 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
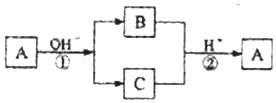
| A. | X元素可能为Al | B. | X元素可能为金属,也可能为非金属 | ||
| C. | 反应①和②互为可逆反应 | D. | 反应①和②一定为氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 20℃,1.01×105Pa下 11.2LN2含有的分子数为3.01×1023 | |
| B. | 4℃时9mL水和标准状况下11.2L氮气含有相同的分子数 | |
| C. | 同温同压下,lmol NO与lmol N2和O2的混合气体的体积不相等 | |
| D. | 0℃、1.01×10sPa时,11.2L氧气所含的原子数目为3.01×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com