
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量NaOH固体样品,溶入水中,再滴加 | NaOH已变质 |
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量NaOH固体样品,溶于水中,再加入 | 该瓶NaOH已全部变质 | |
| 在上述滤液中滴加 |


 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 向含Fe2+、I-、Br-的溶液中通入过量的氯气.溶液中四种粒子的物质的量变化如图所示.已知b-a=5;线段IV表示一种含氧酸,且I和IV表示的物质中含有相同的元素.
向含Fe2+、I-、Br-的溶液中通入过量的氯气.溶液中四种粒子的物质的量变化如图所示.已知b-a=5;线段IV表示一种含氧酸,且I和IV表示的物质中含有相同的元素.查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| △ |

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| △ |

查看答案和解析>>
科目:高中化学 来源: 题型:
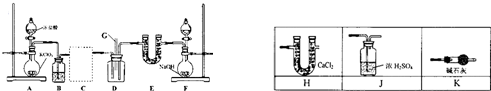
 某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如图所示:
某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、回收并合理处理废电池 |
| B、将煤转化为水煤气作燃料 |
| C、发电厂的煤经脱硫处理 |
| D、电镀废液经中和后直接排放 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com