
| A、棉花、木材和植物秸秆的主要成分都是纤维素 |
| B、含钙、钡、铂等金属元素的物质有绚丽的颜色,可用于制造焰火 |
| C、PM 2.5亦称可入肺颗粒物,分散在空气中形成胶体,表面积大,能吸附有毒有害物质 |
| D、水结冰是从上向下,而油脂凝固是从下向上进行,这一现象合理的解释是因为油脂密度大于水的密度 |


 活力课时同步练习册系列答案
活力课时同步练习册系列答案 学业测评一课一测系列答案
学业测评一课一测系列答案科目:高中化学 来源: 题型:
A、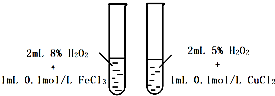 探究不同催化剂对H2O2分解速率影响 |
B、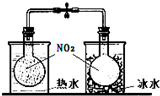 探究温度对2NO2?N2O4平衡影响 |
C、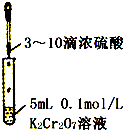 验证Cr2O72-+H2O?2CrO42-+2H+平衡状态变化 |
D、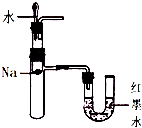 验证钠和水反应的热效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
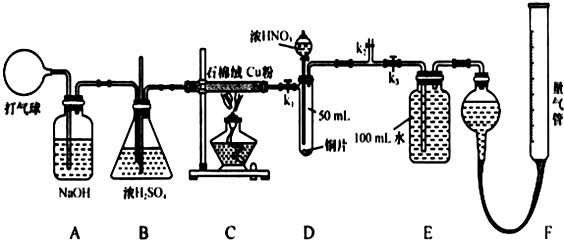
查看答案和解析>>
科目:高中化学 来源: 题型:
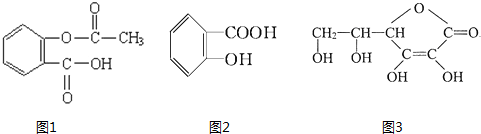
查看答案和解析>>
科目:高中化学 来源: 题型:
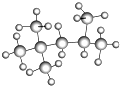 的名称(系统命名法)是
的名称(系统命名法)是查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、Mg2+、SO42-、OH- |
| B、Na+、H+、Cl-、HCO3- |
| C、K+、Ag+、NO3-、Cl- |
| D、K+、Cu2+、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
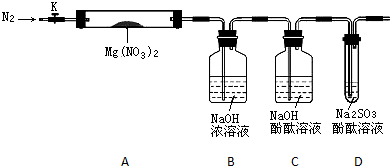
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com